Deze richtlijn beschrijft de te nemen maatregelen en te verrichten onderzoeken na een seksaccident.
NB. Er is een samenvattingskaart van deze richtlijn beschikbaar bestand onder de Bijlagen. Dit is een pdf-bestand op A3-formaat.
Vastgesteld (Landelijk Overleg Infectieziektebestrijding-Seksuele Gezondheid): 28 januari 2020. Gepubliceerd: 23 april 2020.
Wijzigingen sinds vaststelling:
- 20 november 2025: de richtlijn is aangepast conform het actuele chlamydiatestbeleid.
- November 2023: er bleek een pijl te ontbreken in het stroomschema; deze is toegevoegd.
Herziening 2017-2020
Tijdens de herziening in 2017-2020 is een werkgroep van experts enkele keren (fysiek en telefonisch) bij elkaar gekomen waarbij, aan de hand van een aantal onderzoeksvragen die voortkwamen uit een knelpuntinventarisatie, de stand van zaken met betrekking tot het oude draaiboek seksaccidenten (versie 2013) is doorgenomen. De inhoud is hierop aangepast, en de benaming is veranderd naar Richtlijn Seksaccidenten. De opbouw met stappenplan is voortgezet.
Leden werkgroep herziening 2017-2020
- Dr. H.M. Götz, voorzitter, arts M&G, infectieziektebestrijding, (Gemeentelijke gezondheidsdienst) Rotterdam-Rijnmond
- Drs. C. de Boer, arts infectieziektebestrijding, GGD Rotterdam-Rijnmond & GGD Zuid-Holland Zuid
- Prof. dr. K. Brinkman, Nederlandse Vereniging van HIV Behandelaren
- Dr. E.H. Gisolf, Nederlandse Vereniging van HIV Behandelaren
- Drs. R.E. Joosten, arts M&G i.o., infectieziektebestrijding, Centrum Infectieziektebestrijding, (Rijksinstituut voor Volksgezondheid en Milieu)
- Prof. dr. A.C.M. Kroes, Nederlandse Vereniging voor Medische Microbiologie, Werkgroep Klinische Virologie
- Dr. G.G.C. van Rijckevorsel, arts M&G, infectieziektebestrijding, Centrum Infectieziektebestrijding, RIVM
- Dr. R.I. Tjon-Kon-Fat, arts infectieziektebestrijding, GGD Rotterdam-Rijnmond & GGD Zuid-Holland Zuid
Commentaarronde
De conceptrichtlijn werd voor commentaar voorgelegd aan de volgende organisaties:
- het Nederlands Huisartsen Genootschap (NHG);
- de Nederlandse Vereniging van HIV Behandelaren (NVHB);
- de Nederlandse Vereniging voor Medische Microbiologie (NVMM);
- de (Nederlandse Vereniging voor Medische Microbiologie) Werkgroep Klinische Virologie;
- het Landelijk Centrum Hygiëne en Veiligheid (LCHV);
- het Centrum Seksueel Geweld;
- Soa Aids Nederland;
- Het Landelijk Overleg Infectieziekten-Seksuele Gezondheid(LOI-SG; vastgesteld 28 januari 2020).
Overzicht belangrijkste wijzigingen herziening 2017-2020
- De richtlijn is nu gericht op de maatregelen die nodig zijn bij seksaccidenten die plaatsvinden korter dan 8 dagen geleden.
- Een schema met een samenvatting van het stappenplan is toegevoegd.
- Een verwijzing naar het Centrum Seksueel Geweld met contactgegevens is toegevoegd.
- De volgorde van het stappenplan en het bijbehorende stroomdiagram is aangepast conform de Landelijke Richtlijn Prikaccidenten.
- Op basis van literatuuronderzoek zijn de transmissierisico's geactualiseerd. Belangrijkste wijzigingen:
- Een detecteerbare viral load voor hiv wordt gedefinieerd als ≥ 200 copies/ml. U=U geldt ook bij seksaccidenten: bij een bron met een ondetecteerbare viral load is er geen (postexpositieprofylaxe)-indicatie.
- Wijziging in het risico bij insertief anaal/vaginaal met/zonder risico verhogende factoren.
- Drie nieuwe categorieën voor transmissierisico's: geen/verwaarloosbaar, laag en hoog.
- Bij de beoordeling van de hiv-status van de blootgestelde is het gebruik van (pre-expositieprofylaxe) toegevoegd. Bij adequaat gebruik van PrEP is er geen PEP-indicatie.
- De beoordeling van de (hepatitis B-virus)-status van de blootgestelde is gewijzigd. Let op: het beleid voor hepatitis B is NIET identiek aan de Landelijke Richtlijn Prikaccidenten:
- Als een blootgestelde volledig gevaccineerd is, maar er is geen titer bepaald, dan wordt blootgestelde beschouwt als beschermd tenzij de bron bewezen HBsAg-positief is. Dan wordt alsnog cito een titer bij blootgestelde bepaald.
- In principe wordt bij een seksaccident alleen immunoglobulines gegeven als het een hoogrisico-accident is met een bron die bewezen HBsAg-positief is en de blootgestelde een bekende non-responder is of een hoge kans heeft non-responder te zijn (immuungecompromitteerd en/of ouder dan 40 jaar).
- De tabel met de groepen met een verhoogd risico op infecties is geactualiseerd. De groep personen afkomstig uit het Caraïbisch gebied is toegevoegd; deze groep heeft geen verhoog risico op hiv.
- Het testbeleid bij de blootgestelde is gesplitst naar diagnostiek gericht op tijdige soa-opsporing en diagnostiek gericht op alleen het seksaccident.
- De acties bij de blootgestelde op hiv zijn samengevat in een nieuwe tabel, waarbij er een PEP-indicatie kan worden gesteld bij de volgende gevallen:
- hoog transmissierisico in combinatie met een bron uit de risicogroep met onbekende hiv-status en behorend tot een risicogroep of een hiv-positieve bron met een detecteerbare viral load;
- laag transmissierisico met risicoverhogende factoren, in combinatie met een bron uit de risicogroep met onbekende hiv-status en behorend tot een risicogroep of een hiv-positieve bron met een detecteerbare viral load.
- De termijn voor nacontrole bij een PEP-indicatie is aangepast van 6 naar 4 maanden (= 3 maanden na afronden PEP), conform de Landelijke Richtlijn Prikaccidenten.
- Conform de Landelijke Richtlijn Prikaccidenten worden geen hiv-nacontroles geadviseerd bij blootgestelden die een negatieve indicatie hebben voor PEP. Dit geldt bij een beleid dat gericht is op het seksaccident zelf; bij tijdige soa-opsporing is een ander testbeleid opgesteld voor blootgestelden.
- Er is een voorbeeld-registratieformulier voor seksaccidenten toegevoegd aan de richtlijn.
Inleiding
Kader van de richtlijn
Deze richtlijn beschrijft de te nemen maatregelen en te verrichten onderzoeken na een seksaccident.
Aan de hand van deze richtlijn kan op een gestructureerde wijze een inschatting gemaakt worden van het risico op infectie met humaan immunodeficiëntievirus (hiv), hepatitis B-virus (HBV), syfilis, chlamydia, gonorroe en zwangerschap ten gevolge van het seksaccident. Zijdelings komen tetanus en hepatitis C aan bod, omdat in uitzonderingssituaties hier risico op kan bestaan. Afhankelijk van het risico worden al dan niet maatregelen geadviseerd: postexpositieprofylaxe (PEP) tegen een hiv- of HBV-infectie, voorkomen van zwangerschap, of testen en behandeling van soa’s.
De richtlijn is bedoeld voor artsen, verpleegkundigen en overige hulpverleners die betrokken zijn bij de afhandeling van de medische en niet-medische aspecten van een seksaccident. Enkele specifieke niet-medische aspecten, zoals forensische afhandeling (aangifte, sporenonderzoek) en psychosociale aspecten, worden ook behandeld. Deze aspecten maken, hoewel geen onderdeel van de infectieziektebestrijding, wel onderdeel uit van de afhandeling van een seksaccident. Een richtlijn blijft echter altijd een hulpmiddel, in de praktijk zullen zich situaties voordoen waarin de richtlijn niet voorziet of waarin van de richtlijn wordt afgeweken. Neem zo nodig contact op met een deskundige voor intercollegiaal overleg. Daarnaast is het in het kader van de uniformiteit en kwaliteit van de beoordeling van belang om de gegeven adviezen regelmatig te toetsen met collega’s.
Seksaccident
Een seksaccident is een recente seksuele blootstelling aan lichaamsvloeistoffen die tot een infectie met een seksueel overdraagbare aandoening (soa) of een zwangerschap kan leiden en waarbij een snelle afhandeling vanwege risico voor HBV en hiv en/of voorkomen van zwangerschap essentieel is. Het betreft oraal, vaginaal en anaal seksueel contact, zowel receptief als insertief, bij zowel vrouwen als mannen, dat korter dan 8 dagen geleden heeft plaatsgevonden. Binnen dit tijdsbestek kunnen nog preventieve maatregelen genomen kunnen worden tegen HBV (tot op dag 7), hiv (< 72 uur) of zwangerschap (< 5 dagen). Na het verstrijken van deze termijn vervalt dit verschil met een regulier soa-consult en een consult voor mogelijk ongewenst zwanger zijn (zie onder).
Een seksaccident kan op veel verschillende manieren plaatsvinden zoals verkrachting, een gescheurd condoom of een eenmalig onveilig maar wel gewenst seksueel contact. Ook onveilig seksueel contact met een recent bekend geworden hiv-positieve bron, zelfs als hiermee tevoren een jarenlange seksuele relatie bestond, kan als seksaccident beschouwd worden.
Als blootgestelde of bron een hoog risico op een soa hebben, ongeacht dit seksaccident, kan het seksaccident aanleiding zijn om een beleid gericht op tijdige opsporing van een soa in te zetten. Zie het LCI-draaiboek Consult seksuele gezondheid, deeldraaiboek 6: testbeleid.
Als er sprake is van regelmatig hoog risico op hiv is er feitelijk een indicatie voor pre-expositieprofylaxe (PrEP) en moet de persoon worden doorverwezen naar een Centrum Seksuele Gezondheid van de GGD of andere zorgverlener die PrEP-zorg levert zoals de huisarts.
Seksaccidenten en reguliere soa-zorg
De afhandeling van seksaccidenten verschilt op diverse punten van een ‘gewoon’ soa-consult. De meeste artsen komen niet regelmatig in aanraking met een seksaccident. Hierdoor ontbreekt de routine om het accident vlot te kunnen afhandelen. Dit kan vooral bij de indicatiestelling voor hiv-PEP een probleem zijn. Dit wordt gecompliceerd door het gegeven dat de bron vaak niet bekend is of niet wil meewerken. Deze factoren leiden ertoe dat preventieve maatregelen moeten worden geïndiceerd op basis van een risico-inschatting van de bron en soms niet meer op tijd uitgevoerd kunnen worden. Daarnaast zijn er regelmatig forensische aspecten waarmee rekening gehouden dient te worden tijdens het consult. Geadviseerd wordt om in voorbereiding op het consult met een meer ervaren (forensisch) arts van een GGD of een Centrum Seksueel Geweld te overleggen.
Voor meer informatie zie ook het LCI-draaiboek Consult seksuele gezondheid, deeldraaiboek 10: seksaccidenten en seksueel geweld.
Seksueel geweld
Een slachtoffer van seksueel geweld kan zich bij zeer veel verschillende hulpverleners en hulpverleningsinstanties melden, zoals GGD-arts (infectieziektebestrijding, soa, forensisch arts, jeugdgezondheidszorg), GGD-verpleegkundige, huisarts, politie en (Spoedeisende hulp) (Eerste Hulp). Daarnaast kunnen allerlei andere professionals hierbij betrokken raken, zoals gynaecoloog, arts-microbioloog, hiv-behandelaar, kinderarts, abortuskliniek, (Geestelijke gezondheidszorg)-instelling, maatschappelijk werk, Veilig Thuis, etc. Vanwege het grote aantal zorgverleners zijn regionale werkafspraken onontbeerlijk.
Sinds 2012 is het eerste Centrum Seksueel Geweld geopend en sinds 1 januari 2018 is er een landelijk dekkend netwerk. In een Centrum Seksueel Geweld werken medische, forensische, seksuologische en psychologische disciplines samen om slachtoffers van aanranding en verkrachting specialistische zorg te geven. Er wordt aandacht besteed aan zowel medische en psychische aspecten als aan juridische aspecten.
Risico’s op infectie en wederkerigheid
De risico’s op infectie na een seksaccident gelden voor alle bij het seksaccident betrokken personen. Het in de richtlijn beschreven stappenplan zal altijd tweemaal doorlopen moeten worden; beide bij het accident betrokken personen worden beurtelings als blootgestelde en bron beschouwd.
Of een seksaccident leidt tot infectie van de blootgestelde (of van de bron) is afhankelijk van:
- de aard van het accident (stap 2);
Welk seksueel contact is er geweest? Vaginaal, oraal of anaal? Insertief of receptief? Waren er risicoverhogende omstandigheden, zoals een ulcererende soa, verwondingen of ruwe seksuele technieken? - de immuun- en infectiestatus van de blootgestelde (stap 3);
Is de blootgestelde al beschermd door vaccinatie of doorgemaakte infectie? Heeft de blootgestelde op dit moment een soa waardoor het risico op transmissie van andere infecties is verhoogd? - de infectiestatus van de bron (stap 4).
Heeft de bron een soa?
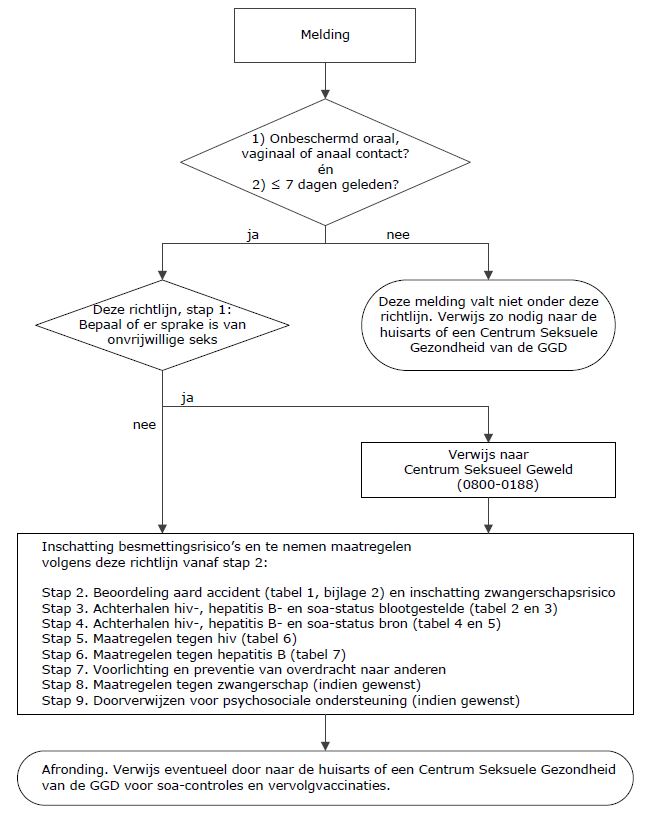
Stroomdiagram richtlijn seksaccidenten
Te gebruiken als ondersteuning.
Figuur: Stroomdiagram
Stappenplan
Een seksaccident is een recente seksuele blootstelling aan lichaamsvloeistoffen die tot een infectie met een seksueel overdraagbare aandoening (soa) of een zwangerschap kan leiden en waarbij een snelle afhandeling vanwege risico voor HBV en hiv en/of voorkomen van zwangerschap essentieel is. Het betreft oraal, vaginaal en anaal seksueel contact, zowel receptief als insertief, bij zowel vrouwen als mannen, dat korter dan 8 dagen geleden heeft plaatsgevonden. Na het verstrijken van deze termijn vervalt dit verschil en is een regulier consult voor soa of voor een mogelijk ongewenste zwangerschap geadviseerd.
Het risico op transmissie van soa is afhankelijk van de aard van het seksaccident (stap 2) en de status van de bron (stap 4).
De risico’s op infectie na een seksaccident gelden voor alle bij het seksaccident betrokken personen. Het in de richtlijn beschreven stappenplan zal altijd tweemaal doorlopen moeten worden waarbij beide bij het accident betrokken personen beurtelings als blootgestelde en bron worden beschouwd.
Stap 1: Onmiddelijke actie
Er is weinig evidence over de effectiviteit en risico’s van desinfecteren na seksuele blootstelling. Desinfecteren van slijmvliezen kan zelfs tot extra beschadigingen aan de slijmvliezen leiden en hiermee juist een verhoogd risico op transmissie van seksuele infecties veroorzaken.
Tetanus
Wanneer bij een seksaccident verwondingen zijn opgetreden waarbij straatvuil in een wond terecht is gekomen (denk bijvoorbeeld aan een verkrachting buiten), dient in voorkomende gevallen beoordeeld te worden of tetanus-postexpositieprofylaxe geadviseerd moet worden. Zie voor meer informatie de LCI-richtlijn Tetanus.
Is er sprake van onvrijwillige seks?
Verwijs dan direct door naar het dichtstbijzijnde Centrum Seksueel Geweld als het slachtoffer dit wil. Het landelijke telefoonnummer voor het Centrum Seksueel Geweld, voor zowel slachtoffers als professionals, is 0800-0188. Vanuit dit centrale nummer zal gekeken worden wat het dichtstbijzijnde centrum is voor het slachtoffer. Let op: de regio die een Centrum Seksueel Geweld bestrijkt, kan afwijken van een GGD-regio.
Het Centrum Seksueel Geweld kan ook in de niet-acute fase adviseren over mogelijkheden van zorg. Bijna elk centrum heeft ook een werkwijze voor subacute meldingen (7-28 dagen geleden) en ook voor latere meldingen.
Indien een slachtoffer niet naar een Centrum Seksueel Geweld wenst te gaan, of indien er sprake is van vrijwillig seksueel contact in de afgelopen 7 dagen, kunnen de stappen van deze richtlijn verder gevolgd worden.
Stap 2: Beoordeling van de aard van het accident
Schat op basis van het seksueel contact het transmissierisico uitgaande van een positieve bron (zie Tabel 1).
- Als het accident geen of een verwaarloosbaar transmissierisico betreft, zijn maatregelen tegen hiv, HBV of soa niet nodig. Ga wel na of de persoon tot een groep met een verhoogd risico voor soa behoort (zie Tabel 4). Verwijs in dat geval de blootgestelde voor een volledig soa-onderzoek naar de huisarts of een Centrum Seksuele Gezondheid van een GGD, of verricht deze zelf. Ga dan naar stap 3.
- Als het accident een laag of hoog transmissierisico heeft, dan moet het stappenplan verder worden doorlopen. Volg dan stap 3 t/m 8.
Als het tijdsinterval tussen het accident en de consultatie langer dan 72 uur tot 7 dagen is, zijn de maatregelen tegen hiv beperkt, na 1 week zijn ook de maatregelen tegen HBV beperkt. De stappen kunnen wel worden doorlopen, om vervangende maatregelen te nemen (bijvoorbeeld actieve vaccinatie tegen HBV en nacontrole). Verwijs hiervoor naar een regulier soa-consult. Zie het LCI-draaiboek Consult seksuele gezondheid, deeldraaiboek 10.
Een snelle beoordeling van het accident is vooral van belang vanwege hiv en HBV, omdat het risico op een infectie met hiv en HBV aanzienlijk kan worden verminderd door het zo snel mogelijk en tijdig inzetten van postexpositiebehandeling.
Bij andere soa’s (syfilis en gonorroe) moet men rekening houden met de incubatietijd; in deze windowfase is een vals-negatieve uitslag mogelijk. Nadat deze periode is verstreken, kan er worden getest en kan zo nodig (vroeg)behandeling worden ingezet. Let op: voor chlamydia geldt sinds januari 2025 een nieuw testbeleid: zonder klachten of zonder partnernotificatie wordt er niet op chlamydia getest.
Waren er risicoverhogende omstandigheden? Vraag na (bij voorkeur bij blootgestelde zelf) wanneer er wat precies gebeurd is. Gebruik indien gewenst het registratieformulier seksaccidenten (zie het voorbeeld registratieformulier seksaccidenten).
Beoordeel op grond van de aard van de seksuele handeling (type blootstelling, met of zonder risicoverhogende factoren) het risico op transmissie voor hiv, HBV, syfilis, chlamydia en gonorroe. Gebruik hierbij Tabel 1. Zie ook de toelichting bij stap 2 (m.n. Tabel 7).
| Type blootstelling | Verwekker | ||
|---|---|---|---|
| Hiv, viral load ≥ 200 copies/ml a | Hepatitis B HBsAg+ | Syfilis, chlamydia, gonorroe | |
| Verkrachting/seksueel misbruik (anaal, vaginaal) b | ++ | ++ | ++ |
| Receptief anaal (geneukt worden) c | ++ | ++ | ++ |
| Insertief anaal (neuken), géén risicoverhogende factoren d | + | ++ | ++ |
| Insertief anaal (neuken), met risicoverhogende factoren d | ++ | ++ | ++ |
| Receptief vaginaal (geneukt worden), géén risicoverhogende factoren d | + | ++ | ++ |
| Receptief vaginaal (geneukt worden), met risicoverhogende factoren d | ++ | ++ | ++ |
| Insertief vaginaal (neuken), géén risicoverhogende factoren d | - | ++ | ++ |
| Insertief vaginaal (neuken), met risicoverhogende factoren d | + | ++ | ++ |
| Oraal e | - | - | + |
| Oraal, met laesies bij infectieuze lues e | - | - | ++ h |
| Contact met feces, urine, speeksel f, zweet | - g | - g | - g |
| (Tong)zoenen | - | - | - |
| Manuele stimulatie of masturbatie met laesies bij infectieuze lues | - | - | ++ h |
| Delen van hulpmiddelen/seksspeeltjes, mits gedesinfecteerd bij wisseling van personen of slechts bij 1 persoon gebruikt | - i | - i | - j |
| Bijt-/krabwonden, als er door huid heen gekrabt en/of gebeten is | ++ k | ++ k | - |
Hepatitis C en andere soa’s
Hepatitis C is niet opgenomen in dit overzicht. Reden hiervoor is dat het risico op seksuele transmissie van het hepatitis C-virus over het algemeen erg klein is. In sommige gevallen kan het wel zinvol zijn om onderzoek naar hepatitis C te doen. Bijvoorbeeld bij (mannen die seks hebben met mannen) na seksaccidenten van zeer ruwe aard (fisting) en/of met veel bloed-bloedcontact en/of met gelijktijdig bestaande soa (hiv, (Lymphogranuloma venereum)). Zie ook de toelichting bij stap 2.
Stap 3: Achterhalen van de hiv-, HBV- en soa-status van de blootgestelde
Bepaal de hiv-, hepatitis B- en soa-status van de blootgestelde. Is blootgestelde nog ontvankelijk voor hiv, hepatitis B of heeft zij/hij naast dit seksaccident eerder risico op een soa gelopen? Dit is van belang voor verder te nemen stappen. Bepaal het testbeleid (zie Tabel 3).
Hiv
Ga anamnestisch na of de blootgestelde op dit moment bekend hiv-seropositief en eventueel onder behandeling is, of hiv-negatief is en PrEP gebruikt.
Beoordeling hiv-status blootgestelde:
- Bekend hiv-seropositief? Verdere maatregelen met betrekking tot hiv bij de blootgestelde zijn niet nodig. Het stappenplan dient wel verder doorlopen te worden ten aanzien van andere infecties/risico’s. Let wel: de blootgestelde die hiv heeft, is mogelijk zelf een bron voor de sekspartner (‘originele’ bron). Achterhaal zo nodig de meest recent bepaalde viral load door, met toestemming van blootgestelde, contact op te nemen met zijn/haar hiv-behandelaar/hiv-behandelcentrum.
- Hiv-status niet bekend? Bepaal cito de hiv-status met een reguliere hiv-test (hiv-p24-antigeen en hiv-antistoffen, een zgn. combotest). Zo nodig kan deze vanwege tijdsgebrek voorafgegaan worden door een hiv-sneltest. Bij een niet-reactieve hiv-sneltest kan voor de beslissing over maatregelen worden uitgegaan van een niet-geïnfecteerd zijnde blootgestelde. Zie ook de toelichting bij stap 3.
- Bekend met gebruik van PrEP? Zie voor medicatieschema’s de HIV Pre-expositie profylaxe (PrEP) richtlijn Nederland. Bij personen die adequaat PrEP gebruiken is er nooit een indicatie voor PEP. Zij worden, indien volgens richtlijn behandeld, sowieso driemaandelijks op hiv getest. Bepaal bij personen die inadequaat hun PrEP gebruiken de hiv-status en volg de stappen van deze richtlijn voor wel of geen indicatie hiv-PEP.
HBV
Ga anamnestisch na of de blootgestelde ooit gevaccineerd is tegen HBV. Op grond van vaccinatiestatus en anti-HBs-respons wordt onderscheid gemaakt tussen beschermden, ongevaccineerden, onvolledig gevaccineerden en non-responders; voor deze groepen geldt een verschillend postexpositiebeleid. Zie Tabel 2.
De blootgestelde wordt als beschermd beschouwd na een complete vaccinatiereeks (ooit 3 vaccinaties). Alleen als de bron HBsAg-drager is, heeft het de voorkeur om bij de blootgestelde na te gaan of de vaccinatie (na complete vaccinatiereeks) tot een adequate anti-HBs-respons heeft geleid (titer anti-HBs ooit > 10 IE/l). Bepaal, als de anti-HBs-titer na vaccinatie onbekend is, cito de HBV-status bij de blootgestelde (anti-HBs, anti-HBc en HBsAg). Bepaling van HBsAg moet met een informed consent gebeuren. Informeer de blootgestelde wat de gevolgen zijn van het aantonen van HBsAg en chronisch dragerschap. Zie de toelichting bij stap 3.
| Blootgestelde | Beoordeling |
|---|---|
| Volledig gevaccineerd, maar geen titer bekend? a | Beschouw als ‘beschermd’, tenzij bron bewezen HBsAg+ is, bepaal dan cito anti-HBs. Anti-HBs ≥ 10 IE/l: beschermd. Anti-HBs < 10 IE/l: afhandeling seksaccident als zijnde een mogelijke non-responder, nu onbeschermd. |
| Volledig gevaccineerd, titer anti-HBs was ooit ≥ 10 IE/l? | Beschermd, ook als bron bekend HBsAg+ is. |
| Volledig gevaccineerd, titer anti-HBs na vaccinatie was < 10 IE/l? | Bekende non-responder (doorgemaakte of aanwezige HBV infectie uitgesloten b), onbeschermd. |
| Eén of twee vaccinaties gehad? De vaccinatieserie moet zo spoedig mogelijk afgemaakt worden. | Mogelijk beschermd/onbeschermd. Bij een bewezen HBsAg-positieve bron, bepaal cito anti-HBs bij blootgestelde. Þ Anti-HBs ≥ 10 IE/l: nu beschermd, zet vaccinatie volgens oorspronkelijk schema voort. Þ Anti-HBs < 10 IE/l: afhandeling accident als zijnde een mogelijke non-responder, nu onbeschermd. Zet daarnaast vaccinatie volgens oorspronkelijk schema voort. b |
| Onbekende vaccinatiestatus? | Beschouw als onbeschermd. |
| Niet gevaccineerd, maar infectie doorgemaakt of bekend met een actieve HBV-infectie? c | Beschermd. |
Beoordeling HBV-immuunstatus blootgestelde:
- Is blootgestelde beschermd tegen HBV? Ten aanzien van HBV zijn geen verdere diagnostiek of maatregelen nodig. Het stappenplan dient wel verder doorlopen te worden ten aanzien van andere infecties/risico’s. Let wel: de blootgestelde met een actieve-HBV infectie (HBsAg+) is zelf een bron voor HBV voor de sekspartner (bron/dader)!
- Is blootgestelde onbeschermd (onvolledig of niet gevaccineerd of een bekende/mogelijke non-responder)? Volg dan stappen 4 t/m 9. Let op: de maatregelen om HBV-infectie te voorkomen, verschillen voor ongevaccineerden en non-responders (zie stap 6).
Soa-testbeleid bij blootgestelde
Afhankelijk of de blootgestelde tot een groep met een verhoogd risico voor soa behoort, wordt een testbeleid afgesproken (zie Tabel 3). Dit kan op verschillende manieren ingestoken worden:
- Beleid gericht op tijdige opsporing van bestaande soa. Als blootgestelde zelf een hoog risico heeft op soa, ook naast dit seksaccident, kan het seksaccident aanleiding zijn om op tijdstip 0 een volledig soa-onderzoek in te zetten. Verricht dan direct een volledig soa-onderzoek (gonorroe bij MSM urine/oraal/anaal, en bij vrouwen afhankelijk van seksueel gedrag ook oraal/anaal; dit geldt ook voor chlamydia indien blootgestelde passende klachten heeft of anderzijds voldoet aan het chlamydia-testbeleid) om soa’s tijdig op te sporen en te behandelen (tijdstip 0). Mocht een blootgestelde de controle-afspraken niet nakomen, dan zijn in ieder geval eerdere soa’s al opgespoord. Inhoudelijk heeft het de voorkeur om vanuit dit soa-bestrijdingsaspect te handelen, vooral als je denkt dat er een zeer hoog risico op een reeds bestaande soa is of als je vermoedt dat client niet terug komt. Een bij het seksaccident opgelopen soa, kan op dat moment echter over het algemeen nog niet aangetoond worden.
- Beleid gericht op het risico van alleen het seksaccident. Dit beleid kan gekozen worden bij een blootgestelde die naast dit seksaccident geen eerder soa-risico heeft gelopen.
| Tijdstip | Beleid gericht op tijdige soa-opsporing bij personen met een verhoogd risico op soa (optie) | Beleid gericht op alleen het seksaccident, geen eerder soa-risico |
|---|---|---|
| Nulmeting | Volg LCI-draaiboek Consult seksuele gezondheid (deeldraaiboek 6: testbeleid) / NHG Standaard: het soa-consult. Bijvoorbeeld MSM-screening:
|
|
| 2(-3) weken na accident f |
|
|
| 3(-6) weken na accident |
|
|
| 3 maanden na accident e |
|
|
| 4-8 weken na 3e HBV-vaccinatie |
|
|
Syfilis
Tegen syfilis zijn geen preventieve maatregelen mogelijk, maar verder onderzoek naar syfilis dient plaats te vinden 3 maanden na het seksaccident. Verwijs de blootgestelde hiervoor door naar de GGD of de eigen huisarts. Bij klachten dient de blootgestelde zich eerder te melden. Syfilis wordt behandeld met antibiotica; de effectiviteit van de behandeling wordt vervolgd met bloedcontroles. Gezien het behandel- en controleschema alsmede de complexiteit van de bloeduitslagen is een nulmeting zinvol wanneer de blootgestelde eerder syfilis heeft doorgemaakt of tot een risicogroep behoort. Zie voor meer informatie de LCI-richtlijn Syfilis.
Chlamydia en gonorroe
Tegen chlamydia en gonorroe kunnen geen preventieve maatregelen genomen worden. Verder onderzoek naar gonorroe dient altijd plaats te vinden, op zijn vroegst 14 dagen na het seksaccident. Verwijs de blootgestelde hiervoor door naar de GGD of de huisarts. Bij klachten dient de blootgestelde zich eerder te melden. Verder onderzoek naar chlamydia vindt plaats conform het chlamydia-testbeleid (zie LCI-draaiboek Consult seksuele gezondheid, deeldraaiboek 6: testbeleid).
Beide infecties zijn goed te behandelen. Preventief antibiotica geven is niet zinvol, tenzij er gekozen wordt voor plaatsing van een morning-afterspiraal, waarmee er wel een indicatie is voor preventieve antibiotica. Het hebben van een soa kan de continuïteit van het slijmvlies onderbreken en als zodanig het risico op transmissie van een andere soa vergroten, wat van belang is voor het inschatten van de transmissierisico’s van syfilis, hiv en HBV. Zie voor meer informatie de LCI-richtlijn Chlamydia trachomatis en de LCI-richtlijn Gonorroe.
Stap 4: Achterhalen van de hiv-, HBV- en soa-status van de bron
Is de bron bekend, beschikbaar en bereidwillig om mee te werken aan brononderzoek? Bij een onbekende of niet-meewerkende bron: bepaal een risicoprofiel van de bron en bepaal of deze afkomstig uit een groep met een verhoogd risico voor hiv, hepatitis B of soa (zie Tabel 4).
Afhankelijk van de aard van het accident en het type blootstelling wordt bij de bron verder onderzoek verricht.
- Vanwege de consequenties voor het verdere beleid bij de blootgestelde is het van belang om snel duidelijkheid te hebben over de hiv en HBV-status van de bron. Stel daarom al het mogelijke in het werk om de bron te achterhalen en uit te vinden of de bron tot een risicogroep behoort. Als er geen bron bekend is moet op grond van de omstandigheden (plaats en context) en andere beschikbare gegevens een inschatting gemaakt worden of de (mogelijke) bron behoort tot een groep met een verhoogd risico voor hiv, HBV of soa (zie Tabel 4).
- Bij een accident met geen of een verwaarloosbaar risico op transmissie van hiv en/of HBV en/of andere soa’s, of als de blootgestelde beschermd is tegen HBV of zelf hiv-seropositief is, kan brononderzoek naar HBV en/of hiv achterwege blijven. Als de bron (of blootgestelde) tot een risicogroep voor soa behoort (zie Tabel 4), verdient het aanbeveling ook deze door te verwijzen naar een Centrum Seksuele Gezondheid of naar de huisarts voor tijdige opsporing van bestaande soa’s.
- Verricht anamnese bij de bron (mogelijk al bekende infectie met soa, risicogedrag, risicogroep, PrEP?). Bij een onbetrouwbare bron, of bij informatie uit de tweede hand: overweeg dossieronderzoek (met toestemming) en/of verder brononderzoek.
- Is de bron bekend met gebruik van PrEP? Zie voor medicatieschema’s de HIV Pre-expositie profylaxe (PrEP) richtlijn Nederland. Wanneer iemand adequaat (volgens richtlijn) PrEP gebruikt, met medische controles, wordt de bron als hiv-negatief beschouwd. Zij worden, indien behandeld, sowieso driemaandelijks op hiv getest. Gebruiken bronnen inadequaat hun PrEP? Bepaal dan de hiv-status bij de bron.
- Vraag op indicatie laboratoriumonderzoek aan. Uitslagen van de cito testen voor hiv en/of HBsAg zijn de basis voor het postexpositiebeleid. Er hoeft niet gewacht te worden op een confirmatietest (in de regel binnen een week bekend).
- Geef de bron informatie waarom onderzoek noodzakelijk is en vraag hiervoor toestemming. Zie hieronder bij ‘Brononderzoek en informed consent’ en de toelichting bij stap 4.
- Indien bij de bron hiv en/of HBV en/of een soa gevonden wordt, dient deze conform de desbetreffende protocollen/richtlijnen verwezen en behandeld te worden.
- Het is niet zinvol om sporen van de bron (sperma of bloed bijvoorbeeld) die gevonden zijn bij de blootgestelde te onderzoeken op hiv, HBV, chlamydia, gonorroe of syfilis. De onderzoeksmethoden zijn hiervoor niet gevalideerd en een negatieve uitslag is niet betrouwbaar.
Testbeleid bij de bron
Bij elk onvrijwillig seksueel contact
- Hiv, cito, liefst binnen 2 uur met een reguliere hiv-screeningstest (anti-hiv en p24) als postexpositieprofylaxe overwogen wordt.
- HBsAg, cito, liefst binnen 24 uur.
- Overige soa-screening op gonorroe en syfilis.
In de praktijk is het echter zelden mogelijk direct na een onvrijwillig seksueel contact onderzoek bij de bron te verrichten, en zal postexpositiebehandeling voor hiv en HBV moeten worden ingezet op grond van risico-inschatting van de bron. Zie hiervoor Tabel 4.
Bij vrijwillig MSM-contact
- Hiv:
- Bron bekend hiv-seropositief en niet behandeld? Neem de maatregelen volgens stap 5.
- Is bron bekend hiv-seropositief en onder behandeling? Adequate behandeling van hiv-infectie leidt tot een niet-detecteerbare viral load (< 200 copies/ml). Achterhaal de meest recent bepaalde viral load door met toestemming van de bron contact op te nemen met zijn/haar hiv-behandelaar/hiv-behandelcentrum. Als dat niet mogelijk is en de bron heeft een duidelijk verhaal over de viral load-status (wanneer laatste gemeten, hoe vaak, hoe is medicatietrouw?) kan een besluit genomen worden op grond van anamnestische gegevens.
- Viral load < 200 copies/ml? Dan beschouwen als niet-besmettelijk.
- Viral load ≥ 200 copies/ml? Dan beschouwen als besmettelijk. Neem de maatregelen volgens stap 5.
- Is de hiv-status niet bekend? Dan brononderzoek op hiv met een reguliere hiv-test (hiv-p24-antigeen en hiv-antistoffen, een zgn. combotest), cito, liefst binnen 2 uur als postexpositieprofylaxe overwogen wordt. Zie ook de toelichting bij stap 4.
- HBsAg:
- Is blootgestelde beschermd tegen HBV of wordt er direct gestart in het kader van het landelijke programma vaccinatie HBV-risicogroepen met vaccinaties tegen HBV (zie stap 3)? Dan is geen verder HBV-brononderzoek nodig.
- Is de blootgestelde een bekende HBV-non-responder (zie stap 3)? Bepaal dan cito (liefst binnen 24 uur) HBsAg bij de bron, maar ...
- Ga eerst anamnestisch na of de bron op dit moment bekend HBsAg-positief is, en of de bron onder behandeling is.
- Ga ook na of de bron gevaccineerd is tegen HBV en/of eerder gescreend (anti-HBC) is op het doormaken van HBV.
- Overige soa’s: screening op anale LGV, gonorroe en syfilis.
Bij vrijwillig heteroseksueel contact
- De bron wordt uitsluitend getest op hiv en/of HBV als deze tot een risicogroep voor hiv of HBV behoort (zie Tabel 4) én als er daadwerkelijk risico op transmissie was, m.a.w. alleen als dit gevolgen heeft voor de te nemen maatregelen bij de blootgestelde.
- Overige soa’s, zoals chlamydia, gonorroe en syfilis, worden getest volgens het reguliere testbeleid (zie LCI-draaiboek Consult seksuele gezondheid, deeldraaiboek 6: testbeleid / NHG Standaard: het soa-consult).
| Aandoening | Welk onderzoek? | Afnamemateriaal |
|---|---|---|
| Hiv a | reguliere hiv-screeningstest (anti-hiv en p24, indien positief confirmatietest (PCR- of immunoblottesten) | serum |
| HBV a,b | HBsAg c | serum |
| Overige soa’s | chlamydia-PCR en gonorroe-PCR syfilis-serologie | wattenstok serum |
Onbekende of niet-meewerkende bron
Wanneer de bron niet beschikbaar is of niet instemt met het brononderzoek, of als de uitslag niet tijdig bekend is, moet op grond van de omstandigheden (plaats en context) en andere beschikbare gegevens een inschatting gemaakt worden of de bron behoort tot een groep met een verhoogd risico voor hiv, HBV of andere soa-infecties (zie Tabel 4). Probeer zoveel mogelijk gegevens van de (mogelijke) bron te achterhalen om op deze wijze toch een risicoprofiel van de bron te kunnen opstellen. Tabel 4 is indicatief en bedoeld om een afweging te maken op basis van achtergrond-prevalenties. Voor meer informatie over een niet-meewerkende bron verwijzen wij u naar toelichting bij stap 4.
| Groep | HBV | Hiv | Chlamydia | Gonorroe | Syfilis |
|---|---|---|---|---|---|
| Mannen die seks hebben met mannen | + | + | + | + | + |
| Sekswerkers (m/v) | + | + b | + | + | + |
| Intraveneuze drugsgebruikers | + | + | + | + | + |
| Personen afkomstig uit Sub-Sahara-Afrika | + | + | + | + | + |
| Personen afkomstig uit Caraïbisch gebied | + | - | + | + | + |
| Personen afkomstig uit Zuidoost-Azië | + | - | + | + | + |
| Personen afkomstig uit Oost-Europa | + | - | + | + | + |
| Personen afkomstig uit overige niet-Westerse landen | + | - | + | + | - |
| Jongeren t/m 24 jaar (Westers) | - | - | + | -/+ c | - |
Brononderzoek en informed consent
Nader onderzoek bij de bron vereist informed consent in het kader van de WGBO (Wet Geneeskundige Behandelingsovereenkomst). Dit kan geregistreerd worden in een eigen dossier van de bron.
Bespreek de consequenties van het verlenen van toestemming: de blootgestelde zal uit het ingestelde beleid de uitslagen van de onderzoeken kunnen afleiden. Bespreek ook de consequenties van het weigeren van toestemming. Probeer de bron ervan te overtuigen dat het toch zinvol is om mee te werken. Mogelijk kan een onnodige behandeling met hiv-PEP worden voorkomen en de blootgestelde krijgt zo eerder zekerheid. Zie voor meer informatie de toelichting bij stap 4 en het voorbeeld van een informed consent-formulier.
Stap 5: Maatregelen tegen hiv
De maatregelen tegen hiv (zie Tabel 5) zijn afhankelijk van:
- de aard van het seksaccident (stap 2): is het risico op transmissie hoog, laag of verwaarloosbaar? Wanneer er geen of een verwaarloosbaar risico op transmissie bestaat, hoeven er geen maatregelen getroffen te worden;
- de hiv-status van de blootgestelde (stap 3): het wordt aanbevolen om voorafgaand aan het starten met PEP bij de blootgestelde een cito hiv-bepaling (< 2 uur) uit te voeren om eerdere infectie bij de blootgestelde uit te sluiten voordat de behandeling gestart wordt; bij blootgestelde personen die hiv-positief testen of adequaat PrEP gebruiken zijn geen maatregelen nodig; het wachten op een uitslag of het ontbreken van nulserum is echter nooit een reden om de start van behandeling uit te stellen tot na de gestelde termijn (< 72 uur na het accident);
- de hiv-status van de bron (stap 4): bij hiv-seropositiviteit van de bron of het behoren tot een risicogroep (zie Tabel 4) wordt sneller overgegaan tot het adviseren van PEP dan in andere gevallen; bij een hiv-positieve bron weegt de viral load in de besluitvorming mee, overleg hierover eventueel met een hiv-behandelaar.
Postexpositieprofylaxe ter preventie van hiv (PEP)
PEP dient zo spoedig mogelijk gestart te worden, liefst binnen 2 uur na het accident, en uiterlijk tot 72 uur na het accident. Na deze termijn is het geven van PEP niet zinvol meer. Het advies is dus te starten met PEP en niet te wachten op een laboratoriumuitslag van de bron dan wel de blootgestelde. Na het beschikbaar komen van een negatieve hiv-uitslag van de bron kan alsnog gestopt worden met PEP. Correct gebruik van PEP heeft geen invloed op resistentieontwikkeling bij eventueel aanwezig hiv-virus; ook een mogelijke (niet aangetoonde) reeds bestaande hiv-besmetting bij de blootgestelde is geen reden om af te zien van het starten met PEP. Het is wel een reden om zo snel mogelijk te verwijzen naar een hiv-behandelaar voor het verdere beleid.
Indicaties
- Bij accidenten met een hoog risico op transmissie én
- een bewezen positieve bron met een detecteerbare viral load (≥ 200 copies/ml);
OF - een bewezen positieve bron met een onbekende viral load;
OF - status bron onbekend maar bron behorend tot groep met een verhoogd risico (zie Tabel 4).
- een bewezen positieve bron met een detecteerbare viral load (≥ 200 copies/ml);
- Bij accidenten met een laag risico op transmissie mét risicoverhogende factoren én
- een bewezen positieve bron met een detecteerbare viral load (≥ 200 copies/ml);
OF - een bewezen positieve bron met een onbekende viral load;
OF - status bron onbekend maar (mogelijke) bron behorend tot groep met een verhoogd risico (zie Tabel 4).
- een bewezen positieve bron met een detecteerbare viral load (≥ 200 copies/ml);
| Risico-inschatting | Bron | ||||
|---|---|---|---|---|---|
| Hiv-positief, met niet-detecteerbare viral load a | Hiv-positief, met onbekende of detecteerbare viral load a | Hiv-status onbekend, behorende tot risicogroep e | Hiv-status onbekend, niet behorend tot risicogroep e | negatief | |
| Hoog transmissierisico | geen indicatie PEP, geen nacontrole | PEP-indicatie, nacontrole op maand 4 b | PEP-indicatie, nacontrole op maand 4 b | geen indicatie PEP, geen nacontrole | geen actie |
| Laag transmissierisico, mét risicoverhogende factoren | geen indicatie PEP, geen nacontrole | PEP-indicatie, nacontrole op maand 4 b | PEP-indicatie, nacontrole op maand 4 b | geen indicatie PEP, geen nacontrole | geen actie |
| Laag transmissierisico, géén risicoverhogende factoren | geen indicatie PEP, geen nacontrole | in principe geen indicatie PEP c, evt. nacontrole maand 3 d | geen indicatie PEP, evt. nacontrole maand 3 d | geen indicatie PEP, geen nacontrole | geen actie |
| Geen of verwaarloosbaar transmissierisico | geen indicatie PEP, geen nacontrole | geen indicatie PEP, geen nacontrole | geen indicatie PEP, geen nacontrole | geen indicatie PEP, geen nacontrole | geen actie |
PEP dient altijd voorgeschreven te worden door, of onder supervisie van, een hiv-behandelaar. Bespreek daarom bij de (mogelijke) PEP-indicatie (ook bij twijfel) met een hiv-behandelaar en maak afspraken hoe de eerste dosis PEP-behandeling zo snel mogelijk kan worden gestart (bijvoorbeeld via een startpakket op de Spoedeisende hulp) en over verwijzing en controle. Voor informatie over behandeling met PEP en bijwerkingen, zie de richtlijn HIV van de NVHB; zie ook de hiv-behandelcentra.
Wijs de blootgestelde bij een positieve PEP-indicatie, ongeacht of PEP ook werkelijk gestart is of niet, op de symptomen die op kunnen treden bij een acute hiv-infectie. Blootgestelde dient dan direct getest te worden.
Nacontrole na gebruik PEP
Na het gebruik van PEP wordt bij de blootgestelde 4 maanden na het accident (3 maanden na het afronden van PEP) een reguliere hiv-screeningstest uitgevoerd (CDC 2013).
Als er ondanks een PEP-indicatie geen PEP is gebruikt (bijvoorbeeld omdat het accident > 72 uur heeft plaatsgevonden), kan 3 maanden na het accident controle met een reguliere hiv-test (hiv-p24-antigeen en hiv-antistoffen, een zgn. combotest) plaatsvinden. In het kader van vroegopsporing van hiv kan ervoor gekozen worden om óók na 3-6 weken na het incident een reguliere hiv-test uit te voeren (zie ook Tabel 3).
Het interval van 4 maanden (3 maanden na afronden PEP) kan ook langer zijn als er redenen zijn voor een verhoogd risico op een verlate seroconversie (immuunsuppressie blootgestelde, (hepatitis C-virus)-co-infectie bij de bron).
Zie ook de toelichting bij stap 5. Blootgestelden die bij nacontrole met hiv geïnfecteerd blijken te zijn, worden naar een behandelaar verwezen voor verdere diagnostiek, behandeling en/of controle. Zie ook hiv-behandelcentra.
Hiv-pre-expositieprofylaxe (PrEP) na PEP
Bij een MSM die een indicatie voor PEP heeft, is een gesprek over preventief gebruik van hiv-medicatie aangewezen. Voor PrEP-indicatie, zie de HIV Pre-expositie profylaxe (PrEP) richtlijn Nederland.
Geen indicatie voor PEP
Er is geen indicatie voor PEP:
- bij alle accidenten waarbij de bron hiv-negatief is;
- bij alle accidenten waarbij de bron correct PrEP gebruikt;
- bij alle accidenten met een bron met onbekende hiv-status die niet tot een risicogroep behoort;
- bij alle accidenten met een bewezen positieve bron die bekend is met een niet-detecteerbare viral load (< 200 copies hiv-RNA/ml, gemeten in de afgelopen 0-12 maanden); het risico op transmissie is verwaarloosbaar klein en er zijn, na overleg met de behandelaar van de bron, ten aanzien van hiv geen maatregelen nodig (BHIVA 2015, EAGA 2015);
- bij accidenten waar er geen of een verwaarloosbare risico op transmissie; nacontrole kan eventueel aangeboden worden (zie onder);
- bij accidenten met een laag risico op transmissie zonder risicoverhogende factoren; in individuele gevallen kan PEP overwogen worden, evenals nacontrole (zie onder).
De in principe negatieve indicatie voor PEP wordt met de blootgestelde besproken. Desondanks kunnen er omstandigheden zijn waardoor de verantwoordelijke arts kan besluiten toch PEP te geven of een nacontrole bij de blootgestelde te doen (bijvoorbeeld wegens psychosociale redenen). Er kan in individuele gevallen dus PEP worden overwogen en van Tabel 5 worden afgeweken, waarbij het belangrijk is de reden van afwijken zo goed mogelijk te documenteren. In de afweging speelt ook nadrukkelijk mee dat PEP, hoewel zeer zeldzaam, ernstige bijwerkingen kan hebben. Wanneer het risico op hiv-transmissie erg klein is (bijvoorbeeld < 1/1000) worden ook zeldzame bijwerkingen relevant wanneer argumenten pro versus contra van PEP worden afgewogen. De uiteindelijke beslissing om PEP te starten, hangt af van de afweging die gemaakt wordt met zorgverlener én cliënt.
Nacontrole bij blootgestelden die geen indicatie voor PEP hebben
Bij een negatieve indicatie PEP is in principe ook geen nacontrole nodig. In sommige gevallen valt te overwegen een nacontrole na 3 maanden bij de blootgestelde te doen.
Stap 6: Maatregelen tegen HBV
De maatregelen tegen HBV zijn afhankelijk van:
- de aard van het seksaccident (zie stap 2): is het risico op transmissie hoog, laag of verwaarloosbaar? Wanneer er geen of een verwaarloosbaar risico op transmissie bestaat, hoeven er geen maatregelen getroffen te worden;
- de HBV-status van de blootgestelde (stap 3): maatregelen zijn alleen nodig voor blootgestelden die onbeschermd zijn tegen HBV door vaccinatie of eerder doorgemaakte infectie;
- de HBV-status van de bron (stap 4): bij een bewezen HBsAg-positieve bron of het behoren tot een risicogroep (zie Tabel 4) wordt sneller overgegaan tot vaccineren dan in andere gevallen.
Uitzondering op bovenstaande: bij een blootgestelde/bron die behoort tot een risicogroep voor HBV (sekswerkers en MSM) is het aanbevolen om ook bij een negatieve bron of verwaarloosbaar risico te verwijzen naar het Centrum Seksuele Gezondheid van de GGD voor het gratis landelijke vaccinatieprogramma hepatitis B-risicogroepen.
Postexpositieprofylaxe ter preventie van HBV-infectie
Zie Tabel 6. Zie ook de toelichting bij stap 6.
Indicaties voor actieve HBV vaccinatie, volgens schema 0-1-6 maanden
- MSM die nog niet tegen HBV beschermd zijn, worden zo spoedig mogelijk doorverwezen voor vaccinaties. De vaccinaties kunnen toegediend worden via het landelijke vaccinatieprogramma hepatitis B-risicogroepen. Hiermee wordt tevens postexpositiebehandeling ingezet. Het is voor deze groep daarom niet zinvol voor wat betreft HBV verdere acties te ondernemen.
→ Maak de serie bij onvolledig gevaccineerde personen af. - Heteroseksuele accidenten: Onbeschermde personen bij accidenten met een risico op transmissie moeten met spoed en binnen 24 uur (tot max. op dag 7) starten met actieve immunisatie, tenzij de bron bewezen negatief is.
Maar: bij onvrijwillig heteroseksueel contact met een onbekende bron niet behorend tot een risicogroep of vrijwillig heteroseksueel contact is het risico op HBV-infectie zo minimaal dat in het algemeen alleen bij een bewezen HBsAg-positieve bron overgegaan wordt tot vaccineren (zie ook voetnoten b en c bij Tabel 6).
→ Maak de serie bij onvolledig gevaccineerde personen af.
→ Overweeg HBV-vaccinatie bij een blootgestelde die behoort tot risicogroep in het kader van het landelijke vaccinatieprogramma hepatitis B-risicogroepen.
Indicaties voor passieve immunisatie met hepatitis B immunoglobuline (HBIg)
HBIg wordt in principe niet toegediend na een seksaccident. Zie de toelichting bij stap 6. In bijzondere gevallen kan hiervan afgeweken worden, bijvoorbeeld wanneer de blootgestelde een bekende non-responder is én de bron bewezen HBsAg-positief is.
- Bekende non-responders ontvangen alleen passieve immunisatie als de bron bewezen HBsAg-positief is door toediening van HBIg (2 doses met een maand tussenruimte), en geen actieve immunisatie.
- Bij personen die een hoge kans hebben non-responder te zijn (immuungecompromitteerd en/of ouder dan 40) kan ook overwogen worden HBIg toe te dienen, tevens kan een boostervaccinatie worden gegeven, of vaccinatie voortzetten volgens oorspronkelijk schema.
HBIg wordt dan liefst binnen 24 uur, maar uiterlijk op dag 7 na het accident toegediend. De dosering van HBIg is voor volwassenen 500 IE, intramusculair, voor kinderen 8 IE/kg intramusculair. Voor de werkzaamheid van immunoglobuline geldt: hoe sneller toegediend hoe beter, omdat immunoglobulinen alleen vrij virus in serum/lichaamsvocht neutraliseren en niet meer werkzaam zijn wanneer het virus een cel is binnengedrongen. Als het accident na meer dan 24 uur gemeld wordt, kan overwogen worden om alsnog HBIg toe te dienen tot maximaal 7 dagen na het accident.
Nacontrole
Na een onvrijwillig accident is het aanbevolen om tegelijkertijd anti-HBc en HBsAg te bepalen om een infectie uit te sluiten. Als alleen passieve immunisatie heeft plaatsgevonden, moet 1 en 3 maanden na de laatste HBIg-toediening HBsAg en anti-HBc worden bepaald.
Blootgestelden die HBsAg-positief blijken, worden naar een behandelaar verwezen voor verdere diagnostiek, behandeling en/of controle en worden gemeld bij de infectieziektebestrijding van de GGD.
Titerbepaling
Overweeg 4 tot 8 weken na het toedienen van het laatste HBV-vaccin een anti-HBs-bepaling om de immuunrespons op de vaccinatie te meten.
| Risico-inschatting | Bron | |||
|---|---|---|---|---|
| Bron HBsAg-positief | Status bron onbekend, behorende tot risicogroep e | Status bron onbekend, niet behorend tot risicogroep e | Bron HBsAg-negatief | |
| Hoog transmissierisico | vaccinatie a | vaccinatie c | vaccinatie b,c | geen actie d |
| Geen of verwaarloosbaar transmissierisico | geen actie d | geen actie d | geen actie d | geen actie d |
Stap 7: Voorlichting en preventie van transmissie naar anderen
De voorlichting is afhankelijk van de infecties waarop getest wordt en waarop reëel risico bestaat. Ten aanzien van seksuele partners geldt dat seks met condoom altijd geadviseerd moet worden. Afhankelijk van welke risico’s gelopen zijn en of PEP gegeven is, kan deze termijn variëren tussen 14 dagen, 3 of 4 maanden na het accident. Voor gezinsleden en het werk geldt dat geen extra maatregelen genomen hoeven te worden. Zie hiervoor ook de richtlijnen per aandoening.
Stap 8: Maatregelen bij mogelijke zwangerschap
Bij onbeschermd vaginaal seksueel contact bestaat het risico op een ongewenste zwangerschap. Er zijn bestaan verschillende mogelijkheden om het risico op zwangerschap te verkleinen, zoals morning-afterpil of de noodspiraal.
Meer informatie over te nemen maatregelen bij mogelijke zwangerschap is te vinden in het LCI-draaiboek Consult seksuele gezondheid, deeldraaiboek 11: anticonceptie en in de NHG standaard Anticonceptie.
Stap 9: psychosociale begeleiding
Hoewel psychosociale hulpverlening niet tot de kerntaken van de infectieziektebestrijding behoort, is het wel een onlosmakelijk onderdeel bij de behandeling en beoordeling van een seksaccident. Het verdient dan ook zeker aandacht.
Bij een Centrum Seksueel Geweld wordt uitgebreid aandacht besteed aan de psychosociale begeleiding na een onvrijwillig seksaccident. Bespreek met een slachtoffer van een onvrijwillig seksaccident of hij/zij contact wil met een hulpverlener van een Centrum Seksueel Geweld in de buurt.
Bij elk seksaccident moet serieus omgegaan worden met gevoelens, emoties en vragen van de blootgestelde. Iedere blootgestelde gaat hier anders mee om. Waar de ene persoon geen behoefte heeft aan gespecialiseerdere hulpverlening, heeft de andere persoon hier juist wel behoefte aan. Het is daarom belangrijk om altijd na te gaan wat de behoeftes zijn van de blootgestelde op dit moment. Ook wanneer de blootgestelde hier nu geen behoefte aan heeft, is het belangrijk dat hij/zij op de hoogte gesteld wordt dat er mogelijkheden zijn, ook als hij/zij zich op een later moment bedenkt.
Soms kan de begeleiding geboden worden door degene die de onderzoeken verricht heeft en de eerste opvang heeft gedaan, maar het is ook mogelijk dat doorgestuurd moet worden naar een gespecialiseerde hulpverlener. Het verdient aanbeveling hier regionaal afspraken over te maken. Voor nazorg bestaat voor bepaalde doelgroepen specifieke hulp; dit varieert van zelfhulpgroepen tot professionele begeleiding. Zie ook het hoofdstuk Nuttige contactgegevens en links.
Toelichting en verantwoording
Begripsbepaling
Mogelijk infectieuze lichaamsvloeistoffen
Hiertoe worden de lichaamsvloeistoffen gerekend die een seksueel overdraagbare infectie kunnen overdragen. De bij een seksaccident betrokken mogelijk infectieuze lichaamsvloeistoffen zijn: sperma, voorvocht, vaginale secretie, bloed en speeksel.
De bron
De persoon wiens mogelijk infectieuze lichaamsvloeistoffen, rechtstreeks of via materiaal, in direct contact zijn gekomen met een andere persoon (lees: ‘de blootgestelde’).
De blootgestelde
De persoon die in contact is gekomen met mogelijk infectieuze lichaamsvloeistoffen van een ander persoon (lees: ‘de bron’).
Hij/zij
In deze richtlijn is bewust gekozen om overal hij/zij te gebruiken. Bij een seksaccident kunnen zowel mannen als vrouwen de blootgestelde zijn en kunnen zowel mannen als vrouwen de bron zijn.
Insertief
Insertief betekent letterlijk: ‘invoegend, instekend’. Hiermee wordt in deze richtlijn de seksuele handeling bedoeld waarbij een penis in de mond, vagina of anus van de ander binnendringt. Ook wordt gesproken over ‘degene die neukt’. In bijzondere gevallen kan het ook betrekking hebben op seksspeeltjes, zoals een dildo.
Voorbeeld: insertief vaginaal contact heeft betrekking op diegene die met zijn penis de vagina binnendringt. Bij anaal seksueel verkeer wordt ook vaak over ‘top’ en ‘bottom’ of ‘actief’ en ‘passief’ gesproken. In dit geval betreft het de ‘top’ of ‘actieve’ partij.
Receptief
Receptief betekent letterlijk ‘ontvangend’. In deze richtlijn wordt met insertief de seksuele handeling bedoeld waarbij een persoon in zijn/haar mond, vagina of anus de penis van een ander persoon ontvangt. Ook wordt gesproken over ‘degene die geneukt wordt’. In bijzondere gevallen kan het ook betrekking hebben op seksspeeltjes, zoals een dildo.
Voorbeeld: receptief vaginaal contact heeft betrekking op diegene die in haar vagina een penis laat binnendringen. Bij anaal seksueel verkeer wordt ook vaak over ‘top’ en ‘bottom’ of ‘actief’ en ‘passief’ gesproken. In dit geval betreft het de ‘bottom’ of ‘passieve’ partij.
Hoog risico/laag risico
Bij de risico-inschatting van een seksaccident is het belangrijk een verschil te maken tussen hoog en laag risico. Let wel: dit is telkens een verwekker-specifieke risico-inschatting (zie Tabel 1). Zo is een hoog risico bij hiv maximaal 3%, terwijl een hoog risico bij gonorroe oploopt tot boven de 50%.
Risicogroepen
In een risicogroep komen bepaalde soa’s meer voor. Dit wil niet zeggen dat personen in een risicogroep ook automatisch risicogedrag vertonen, maar wel dat de a priori kans om iemand te treffen met een bepaalde aandoening groter is.
Risicogedrag
Onder risicogedrag wordt seksueel gedrag verstaan waarbij er makkelijk transmissie van een soa kan optreden.
Risicohandeling
De seksuele handeling die risicovol is voor het oplopen van een bepaalde aandoening. Per soa kunnen dit andere handelingen zijn.
Centrum Seksuele Gezondheid
In veel regio’s worden soa-consulten uitgevoerd op het Centrum Seksuele Gezondheid van de GGD. Dit vindt plaats binnen de subsidieregeling Aanvullende Seksuele Gezondheidszorg en conform het landelijke testbeleid gericht op tijdige opsporing van bestaande soa’s (zie LCI-draaiboek Consult seksuele gezondheid, deeldraaiboek 6: testbeleid).
Er zijn ook andere reguliere zorgverleners die soa-consulten uitvoeren, zoals huisartsen en artsen bij poliklinieken gynaecologie en dermatologie. Wanneer in de tekst over Centrum Seksuele Gezondheid gesproken wordt, wordt de GGD bedoeld.
Toelichting bij stap 2: Beoordeling van de aard van het accident
Inschatten transmissierisico op basis van type blootstelling
Om goed het risico in te kunnen schatten en een weloverwogen keuze te kunnen maken voor het al dan niet nemen van maatregelen, is het noodzakelijk het seksaccident zo volledig mogelijk te inventariseren.
In Tabel 1 is gekozen om het risico op transmissie in de te delen in 3 risicocategorieën: hoog, laag en geen/verwaarloosbaar die corresponderen met de te nemen maatregelen. Tabel 1 is gebaseerd op eenmalige blootstelling. Bij meermalige blootstelling aan een besmettelijke partner is een andere afweging (die buiten deze richtlijn valt) van toepassing.
De indeling is gebaseerd op 3 factoren:
- Het type blootstelling en de hoogte van het risico dat er daadwerkelijk transmissie van pathogenen kan plaatsvinden (voor hiv op basis van inschattingen van diverse meta-analyses; zie Tabel 8). Over het algemeen geldt dat er bij receptief seksueel contact meer risico op transmissie optreedt dan bij insertief contact. Anaal seksueel contact is iets risicovoller dan vaginaal contact. Bij oraal seksueel contact wordt het minste risico gelopen.
- Risicoverhogende factoren, zoals slijmvlieslaesies, bloedbijmenging of besmettelijkheid van de bron, die het risico op transmissie verhogen. Als er risicoverhogende factoren aanwezig zijn, wordt het risico op transmissie hoger geschat, met gevolgen voor de te nemen maatregelen. Bij slijmvliesbeschadigingen is de continuïteit van het slijmvlies onderbroken en bestaat er een verhoogd risico op transmissie van hiv, HBV en syfilis. Deze factoren zijn vrijwel altijd aanwezig bij verkrachting/seksueel misbruik (zowel anaal als vaginaal) en bij receptief anaal seksueel verkeer. De continuïteit van het slijmvlies kan ook onderbroken zijn bij een ulcera, na receptieve anale seks, bij gelijktijdig bestaande (ulcerende) soa, of bij verwondingen ten gevolge van bepaalde seksuele technieken, zoals fisting en sadomasochisme (bijvoorbeeld tepelklemmen, zwepen, naaldhakken). Menstruatiebloed kan hiv, HBV en andere soa’s bevatten. Óf menstruatie bij vaginaal contact als risicoverhogende omstandigheid voor de vrouw moet worden beschouwd, is onbekend. Evidence hiervoor ontbreekt. Voor de vrouw die menstrueert ten tijde van een seksueel contact bestaat er slechts een theoretisch verhoogd risico op het oplopen van hiv of HBV. Vanwege dit theoretische risico kán menstruatie bij vaginaal contact als risicoverhogende factor voor de vrouw worden beschouwd.
- Besmettelijkheid van de bron. Voor hiv en HBV geldt ook dat een hoge hiv-viral load een verhoogde kans op transmissie door de bron geeft. Viral load van hiv ≤ 200 copies/ml geeft geen kans op transmissie (Patel 2014).
In Tabel 7 worden de transmissierisico’s per type blootstelling uiteengezet. Daar waar geen percentages genoemd staan, ontbreken harde cijfers. Tabel 1 is op deze risico’s gebaseerd; in Tabel 7 wordt echter een meer genuanceerde onderverdeling gepresenteerd, waar mogelijk met percentages, omdat hier uiteindelijk de keuze voor de te nemen maatregelen in Tabel 1 mee samenhangt.
| Type blootstelling | Hiv a | HBV b | Chlamydia | Gonorroe | Syfilis c |
|---|---|---|---|---|---|
| Oraal – fellatio insertief | < 0,01% | onbekend | laag | laag | laag c |
| Oraal – fellatio receptief | < 0,01% | onbekend | laag | laag | laag c |
| Oraal – orovaginaal contact | laag | onbekend | laag | laag | laag c |
| Vaginaal – insertief | ≤ 0,1%, ↑ met risicoverhogende factoren | 30% | 25% | 20-30% | gemiddeld |
| Vaginaal – receptief | 0,06-0,19%, ↑ met risicoverhogende factoren | 30% | 50% | 50-70% | gemiddeld |
| Anaal c – insertief | 0,04-0,28%, ↑ met risicoverhogende factoren | hoog | hoog | hoog | hoog |
| Anaal d – receptief | 0,5-3,38% | hoog | hoog | hoog | hoog |
Risico en maatregelen
Bij een hoog en laag risico op transmissie zijn, afhankelijk van de status van de bron, maatregelen nodig ter preventie van hiv, HBV en overige soa’s. De te nemen maatregelen kunnen echter verschillen. Bij geen of een verwaarloosbaar risico op transmissie zijn er geen maatregelen nodig.
De afweging óf (en welke) maatregelen nodig zijn na blootstelling, is gebaseerd op consensus binnen de werkgroep en op internationale en nationale richtlijnen (BASHH 2015, Canadian Guidelines 2017, MDR 2018, NHG 2013). Naast het risico dat er daadwerkelijk transmissie van een pathogeen kan plaatsvinden, spelen ook de mogelijkheden tot interventie en de belasting (bijwerkingen) van de interventie een rol. De mogelijke nadelen van postexpositieprofylaxe moeten altijd worden afgewogen tegen de voordelen.
Onderzoek transmissierisico
Onderzoeken naar het transmissierisico op basis van type blootstelling zijn moeilijk met elkaar te vergelijken, omdat onderzoek is verricht bij verschillende risicogroepen en/of verschillende seksuele technieken. Zo variëren de onderzoeken naar de transmissie van hiv tussen serodiscordante heteroseksuele Afrikaanse koppels en homoseksuele mannen met onveilig receptief anaal seksueel verkeer met anonieme sekspartners in Europa. Ook is er onvoldoende gekeken naar de hoogte van de hiv-load bij transmissierisico’s in deze studies. Bij een hoge load is het risico op transmissie fors hoger. Zie verder Tabel 8.
Ten aanzien van HBV geldt dat geschat wordt dat tussen 16-40% van de vaste seksuele partners van een HBV-drager gedurende de relatie ook geïnfecteerd raakt met HBV. Uit onderzoek blijkt dat HBV eenvoudiger over te dragen valt dan hiv. In een Amerikaans onderzoek komt naar voren dat HBV 8,6 maal besmettelijker is dan hiv (Kingsley 1990). In diverse onderzoeken worden relaties gelegd tussen bepaalde seksuele technieken en het doorgemaakt hebben van HBV. Een precies transmissierisico per sekstechniek wordt echter niet genoemd.
Chlamydia is de meest voorkomende soa in Nederland (60.000 nieuwe infecties per jaar; Slurink 2019). Bovendien is het risico op transmissie per seksueel contact erg hoog: bij een positieve bron bij heteroseksueel receptief vaginaal contact circa 50% en bij insertief vaginaal contact circa 25%. Omdat de consequenties van een chlamydiainfectie lager worden ingeschat dan eerder gedacht is het testbeleid bij de (Centrum Seksuele Gezondheid)’s hier op aangepast (LCI-richtlijn Chlamydia trachomatis en lymfogranuloma venereum, 2024).
Gonorroe komt minder vaak voor, maar is besmettelijker dan Chlamydia; de geschatte transmissierisico’s per seksueel contact met een positieve bron liggen bij heteroseksueel receptief vaginaal contact tussen 50-70% en bij insertief vaginaal contact tussen 20-30% (Van den Broek 2008; LCI-richtlijn Gonorroe, 2018).
Keuze voor verwekkers
In deze richtlijn is een keuze gemaakt om na een seksaccident alleen onderzoek te verrichten naar hiv, HBV, chlamydia, gonorroe en syfilis; de zogenoemde ‘Big Five’. Het advies is gebaseerd op het testbeleid van het Centrum Seksuele Gezondheid (zie LCI-draaiboek Consult seksuele gezondheid, deeldraaiboek 6: testbeleid), wat ook overeenkomt met het testbeleid in de Multidisciplinaire Richtlijn Soa’s (2018) en de NHG Standaard: het soa-consult (2013). Daarnaast is in deze richtlijn de keuze gemaakt om het risico op zwangerschap als onlosmakelijk onderdeel van een seksaccident te zien. De reden hiervoor is om de afhandeling van een seksaccident zoveel mogelijk bij 1 hulpverlener te houden en hierdoor de afhandeling eenvoudiger, sneller en patiëntvriendelijker te laten verlopen. Andere infecties die (ook) seksueel overdraagbaar (kunnen) zijn, zoals hepatitis A, herpes (HSV-1 en (herpessimplexvirus)-2), genitale wratten, candidiasis, trichomonas en humaan papillomavirus, zijn niet in het stappenplan opgenomen vanwege de beperkte preventieve en therapeutische mogelijkheden.
Hepatitis C
Transmissie van hepatitis C via seksueel verkeer lijkt zelden tot nooit voor te komen. Uit een Nederlands onderzoek naar hepatitis C-transmissie bij 50 serodiscordante stellen bleek geen van de partners besmet te zijn geraakt met hepatitis C (LCI-richtlijn Hepatitis C, 2004). Alleen bij seksaccidenten van zeer ruwe aard (fisting) en/of met veel bloed-bloedcontact samen met gelijktijdig bestaande soa (hiv, LGV) met een HCV-positieve bron is er risico op transmissie. Dit wordt bevestigd in Nederlands en Frans onderzoek (Götz 2005, Van de Laar 2007, Gamobotti 2005). Bij heel specifieke groepen, bijvoorbeeld MSM die doen aan receptief anaal contact met ruige sekstechnieken zoals fisten en intraveneus drugsgebruik (slammen), valt het te overwegen om op hepatitis C te testen (Ireland 2017). Ook als er een LGV-infectie bij een eerste test wordt gevonden of wanneer er gestart wordt met hiv-PrEP, is er conform het huidige testbeleid op het Centrum Seksuele Gezondheid een indicatie om te testen op hepatitis C (LCI-draaiboek Consult seksuele gezondheid, deeldraaiboek 6: testbeleid). In andere gevallen lijkt er geen indicatie voor een hepatitis C-test (Fitzpatrick 2017, Hoornenborg 2017).
Toelichting bij stap 3: Achterhalen hiv-, HBV- en soa-status bij blootgestelde
Hiv-onderzoek bij blootgestelde
Hiv-onderzoek bij de blootgestelde gebeurt bij voorkeur met een reguliere screeningstest. Deze bepaling dient altijd cito uitgevoerd te worden, zodat bij een positieve uitslag binnen 2 uur na het accident met PEP gestart kan worden. Als het logistiek niet haalbaar is om binnen 2 uur een hiv-screeningstest te verrichten, kan eerst een hiv-sneltest worden uitgevoerd. Dit vergemakkelijkt de overweging om al dan niet te starten met PEP. Bij een niet-reactieve hiv-sneltest kan voor de beslissing over maatregelen ervan worden uitgegaan dat de blootgestelde niet geïnfecteerd is. Confirmatie-onderzoek is altijd noodzakelijk.
Beschermingsduur HBV-vaccinatie
De Gezondheidsraad stelt dat de duur van de bescherming tegen HBV door de beschikbare vaccins zo lang is als de ervaring ermee. Er zijn geen aanwijzingen dat na een adequate initiële respons na verloop van tijd revaccinatie nodig is. Concreet houdt dit in dat er een goede bescherming tegen HBV bestaat wanneer de titer anti-HBs ooit ≥ 10 IE/l is (zie ook LCI-richtlijn Hepatitis B).
Onvolledig gevaccineerden
Na een seksaccident wordt bij een blootgestelde die slechts 1 of 2 HBV-vaccinaties heeft gehad de vaccinatieserie zo spoedig mogelijk afgemaakt. Overwogen kan worden om anti-HBs te bepalen wanneer er sprake is van een HBsAg-positieve bron en de blootgestelde 2 vaccinaties heeft gehad. In uitzonderingsgevallen (bekende non-responders, bewezen HBsAg-positieve bron) zijn andere maatregelen geïndiceerd.
Na een seksaccident wordt een blootgestelde als beschermd beschouwd na een complete vaccinatiereeks (ooit 3 vaccinaties). Alleen als de bron HBsAg-drager is, heeft het de voorkeur om na te gaan of de vaccinatie (na complete vaccinatiereeks) tot een adequate anti-HBs-respons heeft geleid (titer anti-HBs ooit > 10 IE/l) en de gevaccineerde een mogelijke non-responder is. Bepaal, als de anti-HBs-titer na vaccinatie onbekend is, cito de HBV-status bij de blootgestelde (anti-HBs, anti-HBc en HBsAg). Bij een anti-HBs < 10 IU/l wordt de blootgestelde als mogelijke non-responder beschouwd en wordt HBIg toegediend. Tegelijkertijd kan een boostervaccinatie met HBV-vaccin gegeven worden.
Blootgestelden die HBV hebben doorgemaakt
Als uit de anamnese of eerder laboratoriumonderzoek blijkt dat de blootgestelde niet gevaccineerd is, maar eerder een HBV-infectie heeft doorgemaakt (= anti-HBc-positief en HBsAg-negatief) of nog een actieve HBV-infectie heeft (= anti-HBc-positief en HBsAg-positief, een zgn. drager), kunnen verdere maatregelen ten aanzien van HBV achterwege blijven. Bij twijfel over een doorgemaakte infectie dienen bij de blootgestelde altijd opnieuw alle HBV-markers bepaald te worden. Zie ook bijlage 4 van de LCI-richtlijn Hepatitis B.
Blootgestelden die drager blijken te zijn van hepatitis B
Wanneer blijkt dat de blootgestelde drager is van HBsAg is een doorverwijzing naar een behandelaar (huisarts of internist) noodzakelijk. Mogelijk heeft de bron ook risico gelopen tijdens het seksaccident. Het is wel de taak van de beoordelaar om hierbij stil te staan. Naast HBV kunnen natuurlijk ook andere soa’s gediagnosticeerd worden bij de blootgestelde; hiervoor geldt hetzelfde principe.
Soa-status bij blootgestelde
Het heeft vanuit soa-bestrijdingsperspectief de voorkeur om bij personen die naast dit seksaccident tot een risicogroep behoren voor soa, op tijdstip 0 op soa’s te testen bij een seksaccident.
Uit de studie onder MSM blijkt dat van de personen mét en ook degenen zonder PEP-indicatie 16,5% een soa heeft op tijdstip 0 (De Vrieze 2014). De richtlijnen van de British Association for Sexual Health and HIV adviseren op grond van dit artikel om op tijdstip 0 op soa te testen (BASHH 2015). Indien er geen mogelijkheid is om op tijdstip 0 ter plekke alle soa-diagnostiek in te zetten, dan dient er altijd het advies gegeven te worden dat goede soa-opvolging nodig is, via de huisarts dan wel via de GGD.
Toelichting bij stap 4: Achterhalen van de hiv-, HBV- en soa-status van de bron
Informed consent en recht om niet te weten
In het kader van de Wet op de geneeskundige behandelingsovereenkomst (WGBO) is voor serologisch onderzoek van de bron informed consent (vastgelegd conform de lokale afspraken) noodzakelijk. In het gesprek met de bron dient duidelijk vermeld te worden dat de blootgestelde de uitslag van het bloedonderzoek zal kunnen afleiden uit het al dan niet instellen van maatregelen. Zie ook het voorbeeld van een informed consent-formulier.
Op grond van de WGBO heeft een patiënt ook het recht om van medische onderzoeken af te zien of om uitslagen daarvan niet te vernemen als hij dat niet wil. Het aantonen van hiv- of HBV-infectie kan voor een bronpatiënt naast medische ook vergaande psychosociale consequenties hebben, wat een reden kan zijn om de uitslag van het bloedonderzoek niet te willen weten. Gezien de huidige behandelmogelijkheden en het risico op verspreiding van de ziekte naar zijn/haar omgeving is het gewenst om de bron ervan te overtuigen dat het beter is om de uitslag wel te vernemen en vervolgens adequate maatregelen te nemen.
Brononderzoek bij verdachte van een misdrijf die bloedafname weigert
Als de bron wel beschikbaar is maar bloedafname weigert, dan kan gedwongen afname van bloed plaatsvinden op bevel van de Officier van Justitie met machtiging van de Rechter-Commissaris. Het moet dan gaan om een verdachte van een misdrijf die weigert vrijwillig bloed af te staan en er moet sprake zijn van gerede aanwijzingen dat besmetting door dat misdrijf kan hebben plaatsgevonden. De indicatie voor het bloedonderzoek moet vooraf altijd worden overlegd met een arts die verantwoordelijk is voor de afhandeling van het accident. De uitslag van het bloedonderzoek wordt alleen aan degene die daarom heeft verzocht doorgegeven (zie Wetboek van Strafvordering, artikel 151 f, tweede lid; en zie Besluit bloedtest in strafzaken in geval van een ernstige besmettelijke ziekte op Overheid.nl). NB. Wat betreft de uitvoering kan in de praktijk een arts op grond van ethische bezwaren weigeren om een bloedafname onder dwang uit te voeren (wet BIG).
Beschikbare hiv- en HBV-testen
Bij het testen van een bron kunnen 3 types test een rol spelen:
- De hiv-sneltest is een test die men handmatig ter plekke kan uitvoeren, zonder apparatuur, middels een vingerprik, met in de regel een zeer snel testresultaat. Gevoeligheid en specificiteit zijn in het algemeen iets minder dan bij een reguliere screeningstest. Confirmatie-onderzoek van niet-negatieve uitslagen (dubieus of positief) is altijd noodzakelijk.
- De reguliere HBV- en hiv-test betreft een routinematige, volledig geautomatiseerde serologische screeningstest op aanwezigheid van HBsAg voor HBV-screening; hiv-p24-antigeen en hiv-antistoffen (een zgn. combotest) voor hiv-screening. Confirmatie-onderzoek van niet-negatieve uitslagen (dubieus of positief) is nodig.
- De confirmatietest betreft specialistisch aanvullend onderzoek dat nodig is om een testresultaat, verkregen met een sneltest of een reguliere screeningstest, te bevestigen of te ontkrachten. Het kan bijvoorbeeld gaan om PCR- of immunoblottesten.
Hiv-onderzoek bij de bron
Hiv-onderzoek bij de bron gebeurt bij voorkeur met een reguliere screeningstest. Deze bepaling dient altijd cito uitgevoerd te worden, zodat bij een positieve uitslag binnen 2 uur na het accident met PEP gestart kan worden. Als het logistiek niet haalbaar is om binnen 2 uur een hiv-screeningstest te verrichten, kan eerst een hiv-sneltest worden uitgevoerd. Dit vergemakkelijkt de overweging om al dan niet te starten met PEP. Confirmatie-onderzoek is altijd noodzakelijk.
Bij een negatieve hiv-sneltest moet het onderzoek aan de bron met een reguliere screeningstest (zijnde een combotest) herhaald worden, zodat bij een eventueel fout-negatief testresultaat van de sneltest toch nog tijdig gehandeld kan worden. Dit moet binnen 72 uur na het accident bekend zijn.
Een positieve hiv-sneltest moet altijd met confirmatie-onderzoek bevestigd worden. Dit moet al op de eerstvolgende werkdag geschieden als daarmee achteraf nodeloos gestarte PEP beëindigd zou kunnen worden.
Niet-detecteerbare viral load bij een hiv-positieve bron
Bij een bekende, meewerkende hiv-positieve bron kan de laatst bepaalde hiv-viral load worden opgevraagd om een betere inschatting van het transmissierisico te maken. Met het huidige hiv-behandelbeleid zullen de meeste personen met bekende hiv-infectie met (combinatie antiretrovirale therapie) (combination anti-retroviral therapy) gestart zijn.
Bij goede therapietrouw wordt de viral load ondetecteerbaar. En is er geen risico op transmissie.
Ook bij een hoogrisico-accident (bijvoorbeeld receptief anaal contact met positieve bron) is er geen indicatie tot PEP indien de bron bij de laatste hiv-RNA-meting < 200 copies/ml testte en er goede medicatie-compliance was na deze laatste meting (BHIVA 2015). Dit gaat in overleg met een hiv-behandelaar die bekend is met de geschiedenis en therapietrouw van de persoon (standpunt NVHB).
HBV-onderzoek bij de bron
HBV-onderzoek bij de bron gebeurt door bepaling van HBsAg. Wanneer postexpositiemaatregelen noodzakelijk zijn, zoals HBIg of actieve vaccinatie, is het zinvol om de HBsAg cito aan te vragen. Wanneer alleen gekozen wordt voor actieve vaccinatie is het in de meeste gevallen niet zinvol om dit per direct aan te vragen, maar kan veelal gewacht worden tot de eerstvolgende werkdag. De uitslag zal namelijk nog binnen de gestelde termijn van 7 dagen bekend worden. Zie de toelichting bij stap 6.
Chlamydia, gonorroe en syfilis onderzoek bij de bron
Dit onderzoek hoeft niet cito uitgevoerd te worden, omdat het geen consequenties heeft voor het al dan niet instellen van postexpositiebehandeling. Hier kan soms om psychosociale redenen van afgeweken worden, bijvoorbeeld in het zeldzame geval dat een dader van een verkrachting is opgepakt.
Windowfase: aanvullend brononderzoek bij negatieve uitslagen
Bij een negatieve uitslag van een reguliere hiv-test (hiv-p24-antigeen en hiv-antistoffen, een zgn. combotest) bij een bron die nog in de zogenaamde windowfase verkeert, is het risico op besmetting van de blootgestelde te verwaarlozen. Het is daarom niet nodig om de onderzoeken naar hiv, HBV en gonorroe te herhalen ten behoeve van de blootgestelde. Bij syfilis geldt dit alleen indien er op het moment van het seksaccident geen aanwijzingen waren dat de bron een ulcus had.
Groepen met een verhoogd risico voor hiv, HBV, syfilis en gonorroe
Als de bron niet beschikbaar is voor serologisch onderzoek kan verder beleid worden bepaald door de inschatting of de bron tot een groep met een verhoogd risico voor deze infecties behoort. Op grond van de beschikbare gegevens wordt nagegaan of de bron behoort tot een van de in Tabel 4 genoemde groepen. De tabel is indicatief en geldt voor de Nederlandse situatie; in andere landen kunnen andere risicogroepen bestaan. Het behoren tot een risicogroep houdt niet automatisch in dat iemand risicogedrag vertoont, maar dat de prevalentie van de infectie in die groep hoger ligt dan in de algemene bevolking.
De prevalenties kunnen binnen risicogroepen verschillen. Er zijn onder andere verschillen tussen regio’s, leeftijdsgroepen en stedelijk en niet-stedelijk gebied. Om deze reden moeten zoveel mogelijk gegevens van de bron en blootgestelde worden verzameld en vergeleken met regio-specifieke gegevens om een zo optimaal mogelijke schatting te maken van het risico op hiv-dragerschap van de bron.
Voor hiv maakt de werkgroep een tweedeling in het risico op hiv-dragerschap. Groepen met een hiv-prevalentie van ≥ 10% (Borleffs 2001) worden als groep met een verhoogd risico beschouwd. Dit heeft consequenties voor het te nemen PEP-besluit. Dit is verschillend van het landelijk testbeleid bij GGD en/of huisarts om individuen in het kader van soa-screening op hiv te testen.
- Na een hoogrisico-accident met een niet tijdig te testen bron uit deze categorie wordt PEP aanbevolen.
- Risico hiv, voormalige Nederlandse Antillen. De werkgroep heeft hiv-prevalenties verkregen van de eilanden Curaçao en Sint Maarten en die zijn maximaal 4%. Dit is vergelijkbaar met de omringende eilanden. De werkgroep is van mening dat de hiv-prevalenties op alle eilanden van de voormalige Nederlandse Antillen (Curaçao, Bonaire, Aruba, Sint Maarten, Sint Eustatius, Saba en Aruba) niet hoger zijn dan 4%. Dit betekent dat personen afkomstig uit deze eilanden niet behoren tot een hoog-risicogroep voor hiv in het kader van PEP-beleid.
- Risico hiv, landen uit Sub-Sahara-Afrika. De hiv-prevalentie verschilt per land in Sub-Sahara-Afrika. Voor de meest recente cijfers wordt verwezen naar de website van UNAIDS. Voor een adequate risico-inschatting in de eerste 72 uur is het niet altijd mogelijk om te achterhalen uit welk land in Sub-Sahara-Afrika de bron komt. De werkgroep is van mening dat een bron uit een land uit Sub-Sahara-Afrika behoort tot een risicogroep voor hiv, onafhankelijk van het land waaruit deze bron afkomstig is.
Voor HBV kan voor eerstegeneratiemigranten geboren in niet-westerse landen de volgende geografische indeling worden gebruikt:
- Groepen afkomstig uit landen met een HBsAg-prevalentie ≥ 2% (conform intermediair en hoogendemische gebieden volgens WHO) worden voor HBV als hoogrisicogroep beschouwd (zie ook Traveler’s Health – Hepatitis B op de CDC-website).
Toelichting bij stap 5: Maatregelen tegen hiv
Termijn starten PEP
PEP dient zo spoedig mogelijk gestart te worden, liefst binnen 2 uur na het accident, en uiterlijk tot 72 uur na het accident. (CDC 2016).
Keuze van middelen voor PEP
Voor keuze van middelen voor PEP en de mogelijke bijwerkingen wordt verwezen naar Hoofdstuk 16: transmissiemanagement van de Nederlandse Richtlijn HIV van de NVHB.
Indicatiestelling
In Tabel 1, Tabel 7 en Tabel 8 zijn overzichten te vinden van transmissierisico’s per type blootstelling. In Tabel 5 zijn de indicaties voor PEP samengevat.
Hiv-PEP is geïndiceerd bij incidenten met een risico op transmissie dat hoger uitkomt dan > 0,3% én een bewezen positieve bron met een viral load ≥ 200 copies/ml of een bekende hiv-positieve bron met een onbekende viral load óf bij bron met een onbekende hiv-status maar behorende tot een groep met een hoog risico op seropositiviteit (Tabel 4).
Bij risico’s lager dan 0,3% dient afgezien te worden van PEP. Er kunnen echter redenen zijn waarom toch wordt besloten om PEP te geven of een nacontrole bij de blootgestelde te doen, zoals psychosociale redenen (uitgesproken ongerustheid of angstproblemen die met voorlichting niet kunnen worden weg genomen). Er kan dus in individuele gevallen een andere afweging worden gemaakt en gemotiveerd afgeweken worden van deze richtlijn.
| Type blootstelling | LCI- richtlijn 2020 | Patel 2014 (95%CI) | Baggaley 2018 | BASHH 2015 |
|---|---|---|---|---|
| Oraal – fellatio insertief | < 0,01% | (0-0,04) | < 0,01% (< 1: 10,000) | |
| Oraal – fellatio receptief | < 0,01% | (0-0,04) | < 0,01% (< 1: 10,000) | |
| Oraal – orovaginaal contact | laag | |||
| Vaginaal – insertief | ≤ 0,1%, ↑ met risicoverhogende factoren | 0,04% (0,01-0,04) | 0,08% (1 : 1219) | |
| Vaginaal – receptief | 0,06-0,11%, ↑ met risicoverhogende factoren | 0,08% (0,06-0,11) | 0,10% (1 : 1000) | |
| Anaal – insertief | 0,04-0,28%, ↑ met risicoverhogende factoren | 0,11% (0,04-0,28) | 0,17% (0,09-0,26%) | 0,15% (1 : 666) |
| Anaal – receptief | 0,55-2,23% | 1,38% (1,02-1,86) | 1,25% (0,55-2,23%) | 1,11% (1 : 90) |
PEP, risicogedrag en PrEP
Bij een MSM die een indicatie voor PEP heeft, is een gesprek over preventief gebruik van hiv-medicatie aangewezen. Bij PEP-indicaties is er in feite ook sprake van een PrEP-indicatie. Zie de HIV Pre-expositie profylaxe (PrEP) richtlijn Nederland.
Nacontrole bij een PEP-indicatie
De termijn voor nacontrole is 3 (voorheen 6) maanden na blootstelling (of 4 maanden als PEP is gebruikt = 3 maanden na het beëindigen van PEP), mits de controle is uitgevoerd met een reguliere hiv-screeningstest (= hiv-p24-antigeen en hiv-antistoffen, een zgn. combotest) (CDC 2013, DH 2008). Reden hiervoor is dat er in de literatuur geen gevallen van late seroconversie na 12 weken zijn beschreven (HPA 2005, Wyżgowski 2016).
Een langere follow-up kan geïndiceerd zijn wanneer de blootgestelde immuungecompromitteerd is, of als de bron geïnfecteerd is met zowel hiv als HCV. Er is 1 casus beschreven van een late hiv-seroconversie (na 7 maanden) na een blootstelling aan een hiv-HCV-co-geïnfecteerde bron (Terzi 2007).
Toelichting bij stap 6: Maatregelen tegen HBV
HBV
Er zijn 2 opties voor postexpositieprofylaxe ter preventie van HBV-infectie:
- actieve immunisatie door vaccinatie op maand 0,1 en 6;
- passieve immunisatie door hepatitis B-immunoglobuline (HBIg)-toediening.
Actieve vaccinatie
Over het algemeen voldoet actieve immunisatie vanwege de hoge effectiviteit. HBV heeft een lange incubatietijd. Mogelijk is het virus enige maanden latent aanwezig voor het aanslaat en gaat repliceren. Personen die actief gevaccineerd worden, verkrijgen hun bescherming door de vaccinatie.
Er is weinig onderzoek gedaan naar de effectiviteit van maatregelen tegen HBV bij seksaccidenten. Uit onderzoek naar simultane toediening van vaccin én immunoglobulines blijkt de combinatie het meest effectief. Echter, deze onderzoeken zijn verricht bij verticale transmissie.
Het is aannemelijk te veronderstellen dat bij een seksaccident een relatief kleine hoeveelheid virus wordt overgedragen wat leidt tot een langere incubatietijd dan bij overdracht van een grote hoeveelheid virus. Dit betekent dat er voldoende tijd is om antistoffen te ontwikkelen via vaccinatie.
Actieve vaccinatie heeft een belangrijke plaats binnen de afhandeling van seksaccidenten. Vaccinatie beschermt niet alleen bij een risicovol accident, maar biedt ook in de toekomst bescherming. Dit is dus zeker aan te bevelen wanneer de blootgestelde tot een risicogroep voor HBV behoort (sekswerkers en MSM).
Termijn starten actieve vaccinatie
Post-expositie-vaccinatie geeft niet meteen bescherming. Het duurt enige tijd voor de immuunrespons van de blootgestelde op gang komt. Omdat bij alleen vaccinatie (zonder HBIg) de bescherming geheel afhankelijk is van de respons op vaccinatie wordt hier bij voorkeur binnen 24 uur na het accident met de vaccinatie gestart. Uiterlijk op dag 7. Na deze termijn kan actieve immunisatie wel opgestart worden, maar is de effectiviteit niet goed in te schatten.
Passieve immunisatie met hepatitis B Immunoglobuline (HBIg)
In principe wordt HBIg niet toegediend na een seksaccident. Er is echter een groep waarbij na een hoogrisico-accident (Tabel 1) met een bekende drager van HBsAg toch HBIg geïndiceerd is. Het betreft personen die een bekende non-responder zijn en/of immuungecompromitteerd en/of ouder dan 40 jaar. In de praktijk zal dit een non-responder zijn die onveilig vaginaal en/of anaal seksueel contact heeft gehad met een bewezen (en meewerkende) drager.
Termijn toediening HBIg
HBIg is direct werkzaam en dient voor een maximaal effect binnen 24 uur na mogelijke blootstelling te worden toegediend. Voor immunoglobuline geldt: hoe sneller toegediend hoe beter werkzaam. De immunoglobulinen in HBIg neutraliseren alleen virus als het vrij in serum/lichaamsvocht zit en zijn niet meer werkzaam wanneer het virus een cel is binnengedrongen. Als de HBIg wordt toegediend op maximaal dag 7 na blootstelling, beschermt het in 75% van de gevallen tegen de ontwikkeling van een klinische HBV of een chronische infectie. Toediening na 7 dagen is niet meer zinvol.
Beschermingsduur HBIg
De bescherming van HBIg is slechts tijdelijk. HBIg heeft een halfwaardetijd van 3 weken. HBIg wordt in het lichaam geleidelijk afgebroken en beschermt slechts voor een paar maanden. Als de titer daalt (anti-HBs < 10 IE/l), is iemand weer vatbaar voor infecties. Bij bekende non-responders wordt daarom in geval van een hoogrisico-accident HBIg na 1 maand herhaald. Overige blootgestelden worden in aanvulling op eenmalige HBIg actief gevaccineerd. Een dubbele dosis direct na het accident geeft verlenging van de bescherming met 1 halfwaardetijd, dus 3 tot 4 weken. Een tweede dosis 1 maand na de eerste geeft iets langere tijd bescherming tegen een infectie. Ook de CDC adviseert 2 doses HBIg voor bekende non-responders (CDC 2001).
Serologische nacontrole
Controle vindt plaats om de respons op vaccinatie te meten en eventuele infectie bij de blootgestelde uit te sluiten. Als bij een blootgestelde 1 maand na de laatste HBV-vaccinatie de anti-HBs ≥ 10 IU/l is, is deze persoon beschermd tegen HBV. Tevens wordt anti-HBc en HBsAg bepaald om een infectie uit te sluiten (dit dient met informed consent te gebeuren).
Toediening van HBIg kan interfereren met anti-HBs-bepaling na de oorspronkelijke vaccinatieserie. Stel deze uit tot ten minste 3 maanden na de laatste HBIg-toediening. De halfwaardetijd van HBIg is 3 tot 4 weken. Bij meting van anti-HBs kort na toediening van HBIg worden passieve antistoffen gemeten en geen actief gevormde antistoffen die langdurige bescherming geven.
Als alleen passieve immunisatie (zoals bij een bekende non-responder) heeft plaatsgevonden, moet 1 en 3 maanden na de laatste HBIg, om infectie ten gevolge van het accident uit te sluiten, HBsAg en anti-HBc worden bepaald.
Verklarende afkortingen- en woordenlijst
| Afkorting | Verklaring |
|---|---|
| Anti-HBc | Antistoffen (IgM en (immunoglobuline G)) tegen HbcAg; wijst op oude of recente infectie; niet aanwezig na vaccinatie |
| Anti-HBe | Antistoffen tegen HBeAg |
| Anti-HBs | Indicatie voor passief verkregen antistoffen of immuunrespons na doorgemaakte hepatitis B-infectie of -vaccinatie |
| Anti-HCV | Antistoffen tegen het hepatitis C-virus |
| Anti-hiv | Antistoffen tegen hiv (humaan immunodeficiëntievirus) |
| (Centrum Infectieziektebestrijding) | Centrum voor Infectieziektebestrijding |
| GGD | Gemeentelijke Gezondheidsdienst |
| GGZ | Geestelijke gezondheidszorg |
| cART | combination anti-retroviral therapy |
| HBIg | Hepatitis B-immunoglobuline |
| HBsAg | Hepatitis B-surface-antigeen; indicatie voor een actuele hepatitis B-infectie |
| HBV | Hepatitis B-virus |
| HCV | Hepatitis C-virus |
| Hiv | Humaan immunodeficiëntievirus |
| Insertief | Letterlijk: invoegend, instekend |
| LCI | Landelijke Coördinatie Infectieziekten |
| MSM | Mannen die seks hebben met mannen |
| NVHB | Nederlandse Vereniging van HIV Behandelaren |
| PEP | Postexpositieprofylaxe |
| PrEP | Pre-expositieprofylaxe |
| Receptief | Letterlijk: ontvangend |
| RIVM | Rijksinstituut voor Volksgezondheid en Milieu |
| SEH | Spoedeisende Eerste Hulp |
| Soa | Seksueel overdraagbare aandoening |
| TPPA | Treponema-pallidum particle agglutinatie assay (screening voor syfilis) |
| TPHA | Treponema-pallidum hemagglutinatie-reactie (screening voor syfilis) |
| Viral load | Hoeveelheid virus in bloed |
Nuttige contactgegevens en links
- Centrum Seksueel Geweld. www.centrumseksueelgeweld.nl. Tel: 0800-0188.
- FIOM, stichting die psychosociale hulp en advies biedt bij o.a. ongewenste zwangerschap en tienermoeders. Online biedt FIOM keuzehulp en biedt het de mogelijkheid telefonisch contact te hebben met een hulpverlener. www.fiom.nl.
- GGD, Gemeentelijke of Gemeenschappelijke Gezondheidsdienst. www.ggd.nl.
- Hiv Vereniging Nederland, landelijke vrijwilligersorganisatie voor informatie, onderling contact en ondersteuning en belangenbehartiging.
- Algemeen: www.hivvereniging.nl.
- Overzicht hiv-behandelcentra: www.hivvereniging.nl/hiv-behandelcentra.
- Publieksinformatie over overdracht hiv: www.hivvereniging.nl/hiv-wat-nu/overdracht-van-hiv.
- JIP, Jongeren Informatie Punt. Hier wordt informatie verstrekt aan jongeren; ook kan worden doorverwezen. Het JIP werkt via regionale kantoren. Adressen te vinden via www.jip.org.
- LECK, Landelijk Expertise Centrum Kindermishandeling. https://leck.nu.
- Seksueelgeweld.info, website voor slachtoffers en betrokken van seksueel geweld. www.seksueelgeweld.info.
- LCI, Landelijke Coördinatie Infectieziektebestrijding. https://lci.rivm.nl.
- Movisie, kennis en aanpak van sociale vraagstukken (het voormalige TransAct is hierin opgegaan). Biedt voor de thema’s huiselijk en seksueel geweld o.a. uitgebreide informatie, publicaties, trainingen en foldermateriaal. www.movisie.nl.
- NGVA, Nederlands Genootschap van Abortusartsen. Lijst met abortusklinieken in Nederland: www.ngva.net/klinieken.
- NVHB. Nederlandse Vereniging van HIV Behandelaren. https://nvhb.nl.
- Politie – zedenzaken. Regioafdeling te bereiken via 0900-8844. www.politie.nl.
- RIVM. Rijksinstituut voor Volksgezondheid en Milieu. www.rivm.nl.
- Rutgers, kenniscentrum seksualiteit. Ondersteunt professionals in hun werk rondom seksualiteit. www.rutgers.nl.
- Sense.info, website voor jongeren voor alle vragen rondom soa, seksualiteit, anticonceptie en zwangerschap. Zoekfunctie voor GGD-locaties voor soa-testen. www.sense.info.
- Soa Aids Nederland, expertisecentrum voor hiv/aids en andere soa’s. www.soaaids-professionals.nl.
- Veilig Thuis, advies- en meldpunt huiselijk geweld en kindermishandeling. www.veiligthuis.nl. Tel: 0800-2000.
Literatuur
- Advisory Committee for HIV and STD Prevention. HIV prevention through early detection and treatment of other sexually transmitted diseases – United States: recommendations of the Advisory Committee for HIV and STD Prevention. (Morbidity and Mortality Weekly Report) 1998 Aug;47(RR12):1-24.
- Almeda J, Casabona Barbarà J, Simon B, et al. Proposed recommendations for the management of HIV post-exposure prophylaxis after sexual, injecting drug or other exposures in Europe. Euro Surveill. 2004 Jun;9(6):5-6.
- Baggaley RF, Owen BN, Silhol R, et al. Does per act HIV-1 transmission risk through anal sex vary by gender? An updated systematic review and meta-analysis. Am J Reprod Immunol. 2018 Nov;80(5):e13039.
- Baggaley RF, White RG, Boiley (Medisch Centrum). HIV transmission risk through anal intercourse: systematic review, meta-analysis and implications for HIV prevention. Int J Epidemiol. 2010 Aug;39:1048–63.
- Baggaley RF, White RG, Boiley MC. Systematic review of orogenital HIV-1 transmission probabilities. Int J Epidemiol. 2008 Dec;37(6):1255-65
- BASSH (British Association for Sexual Health and HIV). Guidelines 2015.
- BHIVA (British HIV Association). UK national guideline for the use of HIV post-exposure prophylaxis following sexual exposure (PEPSE) 2015.
- Borleffs JCC, Danner SA, Lange JMA et al. (Centraal Begeleidings Orgaan voor de intercollegiale toetsing)-richtlijn ‘Antiretrovirale behandeling in Nederland’. Ned Tijdschr Geneeskd. 2001;145:1585-9.
- Canadian Guidelines on PrEP & nPEP 2017.
- CDC. Sexually transmitted diseases treatment guidelines, 2015. MMWR 2015 Jun;64(3).
- Cohen MS, Shugars DC, Fiscus SA. Limits on oral transmission of HIV-1. Lancet. 2000 Jul 22;356(9226):272.
- Cresswell F, Waters L, Briggs E, et al. UK guideline for the use of HIV post-exposure prophylaxis following sexual exposure, 2015. Int J STD AIDS. 2016 Aug;27(9):713-38.
- De Vrieze NH, van Rooijen MS, van de Loeff MS, et al. Additional gonorrhea and chlamydia infections found with rapid follow-up screening in men who have sex with men with an indication for HIV postexposure prophylaxis. Sex Transm Dis. 2014 Aug; 41(8):515-7.
- Fitzpatrick C, Pinto-Sander N, Williams D, et al. Acute hepatitis C in HIV-uninfected men who have sex with men who do not report injecting drug use. Int J STD AIDS. 2017 Oct;28(11): 1158.
- Gamobotti L, Acute hepatitis C collaborating group. Acute hepatitis C infection in HIV positive men who have sex with men in Paris, France, 2001-2004. Euro Surveill. 2005 May;10(5):3-4.
- Götz HM, Doornum G van, Niesters HG, et al. A cluster of acute hepatitis C virus infection among men who have sex with men – results from contact tracing and public health implications. AIDS. 2005 Jun;19(9):969-74.
- Hoornenborg E, Achterbergh R, Schim van der Loeff M, et al. Men who have sex with men starting pre-exposure prophylaxis (PrEP) are at risk of HCV infection: evidence from the Amsterdam PrEP study. AIDS. 2017 Jul;31(11):1603-10.
- Ireland G, Higgins S, Goorney B, et al. Evaluation of hepatitis C testing in men who have sex with men, and associated risk behaviours, in Manchester, UK. Sex Transm Infect, 2017 Sep;93(6):404-409.
- Kingsley LA, Rinaldo CR Jr, Lyter DW, et al. Sexual transmission efficiency of hepatitis B virus and human immunodeficiency virus among homosexual men. JAMA. 1990 Jul 11;264(2):230-4.
- van de Laar TJ, van der Bij AK, Prins M, et al. Increase in HCV incidence among men who have sex with men in Amsterdam most likely caused by sexual transmission. J Infect Dis. 2007 Jul 15;196(2):230-8.
- LCI. Draaiboek Consult seksuele gezondheid. Versie 2019.
- LCI. Landelijke Richtlijn Prikaccidenten. Versie 2019.
- MDR. Multidisciplinaire Richtlijn Soa’s. Versie 2018 met update 2019.
- Patel P, Borkowf CB, Brooks JT, et al. Estimating per-act HIV transmission risk: a systematic review. AIDS. 2014 Jun 19;28(10):1509-19.
- NVHB. HIV Pre-expositie profylaxe (PrEP) richtlijn Nederland. Gereviseerde versie 2 (15 april 2019).
- NVHB. Richtlijn HIV. Versie 2019.
- NHG. NHG Standaard: het soa-consult. Versie 2013.
- Slurink IAL, van Aar F, Op de Coul ELM, et al. Sexually transmitted infections in the Netherlands in 2018. RIVM Rapport 2019-0007. RIVM 2019.
- Vandelli C, Renzo F, Romanò L, et al. Lack of evidence of sexual transmission of hepatitis C among monogamous couples: results of a 10-year prospective follow-up study. Am J Gastroenterol. 2004 May;99(5):855-9.
- Waldo CR, Stall RD, Coates TJ. Is offering post-exposure prevention for sexual exposures to HIV-related to sexual risk behaviour in gay men? AIDS. 2000 May;14(8):1035-9.